题目内容
【题目】工业上从铝土矿(主要成分是Al2O3还含有SiO2、Fe203等杂质)中提取铝可采用如图工艺流程(反应条件已经省略):
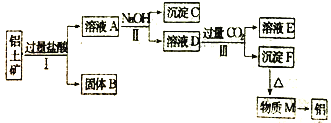
请回答下列问题:
(1)图中I、Ⅱ、Ⅲ步骤中涉及分离溶液与沉淀的实验方法是___________(填操作名称)。
(2)Al2O3是两性氧化物,SiO2是酸性氧化物,Fe2O3是碱性氧化物,根据它们的性质,判断固体B的成分是__________(填化学式)。
(3)Fe2O3和盐酸反应的化学方程式为______________,沉淀C的化学式是__________。
(4)如果溶液D中通入“过量CO2”,改成通入“过量HCl”可以吗? 为什么? ____________________。
【答案】 过滤 SiO2 Fe2O3+6HCl=2FeCl3+3H2O Fe(OH)3 不可以,Al(OH)3和过量的盐酸反应。
【解析】试题分析:本题以铝土矿提取铝的工艺流程为载体,考查流程的分析,方程式的书写,基本实验方法,Al2O3、Fe2O3、SiO2、Al(OH)3的性质。
(1)分离溶液与沉淀的实验方法为过滤。
(2)Al2O3是两性氧化物,SiO2是酸性氧化物,Fe2O3是碱性氧化物,图中I步骤中加入过量的盐酸,发生的反应有:Al2O3+6HCl=2AlCl3+3H2O、Fe2O3+6HCl=2FeCl3+3H2O,SiO2与盐酸不反应,固体B的成分是SiO2。
(3)Fe2O3与盐酸反应生成FeCl3和H2O,化学方程式为Fe2O3+6HCl=2FeCl3+3H2O。溶液A中含有AlCl3、FeCl3和过量HCl,步骤II向溶液A中加入NaOH,发生的反应有:HCl+NaOH=NaCl+H2O、AlCl3+4NaOH=3NaCl+NaAlO2+2H2O、FeCl3+3NaOH=Fe(OH)3↓+3NaCl,沉淀C的化学式为Fe(OH)3。
(4)溶液D中含有NaAlO2、NaCl和NaOH,向溶液D中通入过量CO2发生的反应为:CO2+NaAlO2+2H2O=Al(OH)3↓+NaHCO3、CO2+NaOH=NaHCO3,沉淀F为Al(OH)3。若将“过量CO2”改为“过量HCl”,由于Al(OH)3是两性氢氧化物,Al(OH)3会和过量盐酸反应而溶解,从而使得提取的Al的产量降低,所以不能将“过量CO2”改为“过量HCl”。

