题目内容
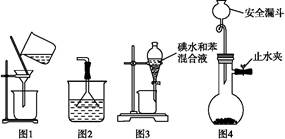
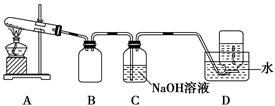
有一混合气体,可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下,取此气体200 mL进行实验,实验的过程和结果如下:
①观察此混合气体为无色。
②将此气体通过浓硫酸,气体体积减少了40 mL。
③将②中剩余的气体,通过Na2O2固体,气体体积变为120 mL。
④将③中剩余的气体引燃充分反应后,冷却至常温,气体体积又减少了105 mL。(上述气体的体积都是相同条件下测定的)。
⑤剩余气体通过加热的铜网,剩余10 mL气体。
根据上述实验,试推断:
(1)混合气体中肯定存在的气体是_________,它们的体积分别为_________。
(2)混合气体中肯定不存在的气体是__________________。
(3)混合气体中可能含有的气体是_________,其体积共为_________。
①观察此混合气体为无色。
②将此气体通过浓硫酸,气体体积减少了40 mL。
③将②中剩余的气体,通过Na2O2固体,气体体积变为120 mL。
④将③中剩余的气体引燃充分反应后,冷却至常温,气体体积又减少了105 mL。(上述气体的体积都是相同条件下测定的)。
⑤剩余气体通过加热的铜网,剩余10 mL气体。
根据上述实验,试推断:
(1)混合气体中肯定存在的气体是_________,它们的体积分别为_________。
(2)混合气体中肯定不存在的气体是__________________。
(3)混合气体中可能含有的气体是_________,其体积共为_________。
(1)H2、NH3、CO2 H2 70 mL、NH3 40 mL、CO2 80 mL
(2)O2、HCl (3)N2和He 10 mL
(2)O2、HCl (3)N2和He 10 mL
此气体通过浓硫酸,气体体积减少了40 mL,说明含有氨气40 mL,有氨气时,氯化氢不能存在;剩余的气体,通过Na2O2固体,气体体积变为120 mL,减少40 mL,由方程式2Na2O2+2CO2====2Na2CO3+O2可知含有CO2 80 mL,同时生成O2 40 mL;再根据剩余的气体引燃充分反应2H2+O2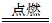 2H2O,冷却至常温,气体体积又减少了105 mL,还有气体15 mL,说明含有氢气70 mL,③中生成的氧气还剩5 mL;剩余气体通过加热的铜网,剩余10 mL气体,减少5 mL气体说明原混合气体中无氧气,剩余10 mL为N2或He或两者的混合物。
2H2O,冷却至常温,气体体积又减少了105 mL,还有气体15 mL,说明含有氢气70 mL,③中生成的氧气还剩5 mL;剩余气体通过加热的铜网,剩余10 mL气体,减少5 mL气体说明原混合气体中无氧气,剩余10 mL为N2或He或两者的混合物。
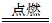 2H2O,冷却至常温,气体体积又减少了105 mL,还有气体15 mL,说明含有氢气70 mL,③中生成的氧气还剩5 mL;剩余气体通过加热的铜网,剩余10 mL气体,减少5 mL气体说明原混合气体中无氧气,剩余10 mL为N2或He或两者的混合物。
2H2O,冷却至常温,气体体积又减少了105 mL,还有气体15 mL,说明含有氢气70 mL,③中生成的氧气还剩5 mL;剩余气体通过加热的铜网,剩余10 mL气体,减少5 mL气体说明原混合气体中无氧气,剩余10 mL为N2或He或两者的混合物。
练习册系列答案
相关题目
 、S
、S 、S
、S 离子中的若干种组成,陶宝同学设计实验检验其组成,记录如下:
离子中的若干种组成,陶宝同学设计实验检验其组成,记录如下: