题目内容
【题目】25℃时,水的电离达到平衡:H2O![]() H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量盐酸,平衡逆向移动,c(OH-)增大
D.将水加热,Kw增大,pH不变,呈中性
【答案】B
【解析】
试题分析:A.向水中加入稀氨水,由于氨水在溶液中存在电离平衡:NH3H2O![]() NH4++OH-,电离产生的OH-使溶液中c(OH-),水的电离平衡逆向移动,c(OH-)升高,错误; B.向水中加入少量固体硫酸氢钠,盐电离产生的H+使溶液中c(H+)增大,温度不变,所以Kw不变,正确;C.向水中加入少量HCl,电离产生的H+,使水的电离平衡逆移动,c(H+)降低,但是平衡移动的趋势是微弱的,溶液中酸电离产生的离子浓度增大的趋势大于平衡移动使离子浓度减小的趋势,所以c(H+)增大,c(OH-)减小,错误;D.将水加热,Kw增大,c(H+)增大,pH减小,溶液仍然呈中性,错误。
NH4++OH-,电离产生的OH-使溶液中c(OH-),水的电离平衡逆向移动,c(OH-)升高,错误; B.向水中加入少量固体硫酸氢钠,盐电离产生的H+使溶液中c(H+)增大,温度不变,所以Kw不变,正确;C.向水中加入少量HCl,电离产生的H+,使水的电离平衡逆移动,c(H+)降低,但是平衡移动的趋势是微弱的,溶液中酸电离产生的离子浓度增大的趋势大于平衡移动使离子浓度减小的趋势,所以c(H+)增大,c(OH-)减小,错误;D.将水加热,Kw增大,c(H+)增大,pH减小,溶液仍然呈中性,错误。

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
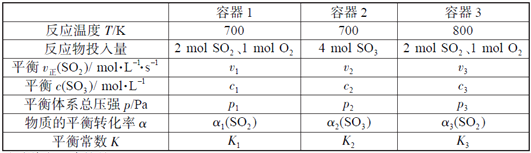
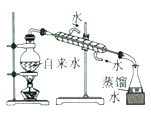
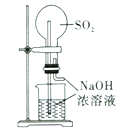
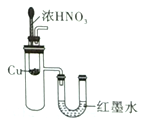
【题目】下列实验装置不能达到实验目的的是
A | B | C | D |
|
|
|
|
实验室制取蒸馏水 | 用SO2和NaOH溶液做喷泉实验 | 证明Na2CO3的热稳定性比NaHCO3好 | 证明铜与浓硝酸的反应是放热反应 |
A. A B. B C. C D. D
【题目】在空气中加热5.49g草酸钴晶体(CoC2O4·2H2O,摩尔质量为183g/mol),受热过程中不同温度范国内分别得到一种固体物质,其质量如下表:
温度范围℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,210℃~290℃过程中产生的气体只有CO2,则290℃~320℃温度范围内的固体物质是
A. CoO B. Co2O3 C. Co3O4 D. Co4O5