题目内容
16.下列事实中,与电化学腐蚀无关的是( )| A. | 减少钢铁中的含碳量,可以增强钢铁的耐腐蚀能力 | |
| B. | 纯银打造的饰品放置一段时间后表面会生成一层黑色物质 | |
| C. | 为保护海轮的船壳,常在船壳上镶入锌块 | |
| D. | 镀银的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀 |
分析 A.钢铁中的含碳量越高,越易与Fe形成原电池,越易发生电化学腐蚀;
B.金属银在空气中发生化学腐蚀生成硫化银而变黑;
C.利用原电池原理保护金属不被腐蚀;
D.根据原电池原理的应用:负极金属的腐蚀速率快于正极上的金属来解答.
解答 解:A.钢铁中的含碳量越高,越易与Fe形成原电池,越易发生电化学腐蚀,和电化学腐蚀有关,故A不选;
B.金属银在空气中能够生成黑色的硫化银而变黑,此过程属于普通化学腐蚀,与电化学腐蚀无关,故B选;
C.在船壳水线以下部分装上锌块,属于牺牲阳极的阴极保护法,与电化学腐蚀有关,故C不选;
D.镀锡的铁制品,镀层部分受损后,露出的铁与锡形成原电池,因为铁的活泼性强于锡,铁做负极,发生氧化还原反应被腐蚀,与电化学腐蚀有关,故D不选;
故选B.
点评 本题考查了金属的腐蚀与防护,注意电化学腐蚀形成条件和知识的归纳综合,题目难度不大.

练习册系列答案
相关题目
6.下列物质组合中,既能和强酸反应又能和强碱反应的物质是( )
①Al ②Al2O3 ③Al(OH)3 ④AlCl3⑤NaHCO3.
①Al ②Al2O3 ③Al(OH)3 ④AlCl3⑤NaHCO3.
| A. | ①②③⑤ | B. | ②③④ | C. | ①②④ | D. | ①② |
7.下列叙述正确的是( )
| A. | 1molH2O的质量为18g•mol-1 | |
| B. | CH4的摩尔质量为16g | |
| C. | 3.01×1023个SO2分子的质量为32 g | |
| D. | 1mol任何物质均含有6.02×1023个分子 |
4.下列叙述正确的是( )
| A. | 直径介于1-100nm之间的微粒称为胶体 | |
| B. | 氢氧化铁胶体是纯净物 | |
| C. | 利用丁达尔效应可以区别溶液和胶体 | |
| D. | 胶体粒子很小,可以透过半透膜 |
4.下列有机化合物分子中,所有碳原子不可能处于同一平面的是( )
| A. |  | B. | CH3-C≡C-CH3 | C. | 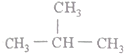 | D. | 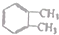 |
8.某化学小组通过査阅资料,设计了如图所示的方法以含镍催化剂为原料来制备NiSO4•7H20.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
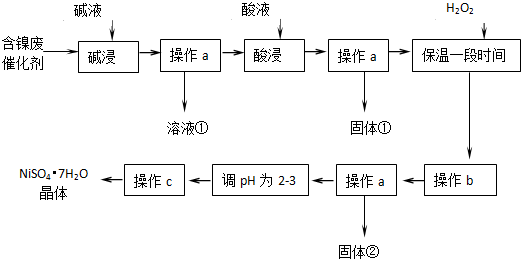
部分阳离子以氢氧化物形式沉淀时的pH如下:
(1)“碱浸”时反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2OH-═2AlO2-+H2O.
(2)“酸浸”时所加入的酸是H2SO4(填化学式).
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M═NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.

部分阳离子以氢氧化物形式沉淀时的pH如下:
| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(2)“酸浸”时所加入的酸是H2SO4(填化学式).
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M═NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
 ;在上述由SiCl4气体制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g);△H=+0.025akJ•mol-1.
;在上述由SiCl4气体制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g);△H=+0.025akJ•mol-1.