题目内容
美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
A.原子半径:Na>Al
B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na)
C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小
D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成
C
【解析】 元素周期表中Na、Al位于同周期,钠的原子序数小于Al,故原子半径:Na>Al,A项正确;Na与水反应生成NaOH,Al与NaOH反应生成NaAlO2,关系式为Na~NaOH~Al,得到无色溶液,说明Na、Al全部溶解,n(Al)≤n(Na),B项正确;失去1 mol电子,消耗Na为23 g,而消耗Al为9 g,故相同质量的Na、Al,后者放出氢气较多,在合金中Al的质量分数越高,放出的氢气就越多,C项错误。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案由某金属的混合物(含65%Cu、25%Al、8%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线设计如下:

已知物质开始沉淀和沉淀完全时pH如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
沉淀开始时pH | 2.7 | 4.1 | 8.3 |
沉淀完全时pH | 3.7 | 5.4 | 9.8 |
请回答下列问题:
(1)过滤操作用到的玻璃仪器有________。
(2)第①步Al与足量酸反应的离子方程式为___________________________,
得到滤渣1的主要成分为________。
(3)第②步用NaOH调节溶液pH的范围为________。
(4)由第③步得到CuSO4·5H2O晶体的步骤是将滤液2________、________、过滤、洗涤、干燥。
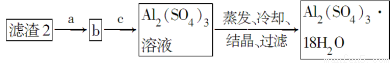
(5)现有洗涤后的滤渣2制取Al2(SO4)3·18H2O,请将a、b、c补充完整。