题目内容
下列各组中的性质比较,正确的是( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:KOH>Ca(OH)2>Mg(OH)2
③稳定性:HCl>H2S>PH3 ④还原性:F-->Cl-->Br--
①酸性:HClO4>HBrO4>HIO4 ②碱性:KOH>Ca(OH)2>Mg(OH)2
③稳定性:HCl>H2S>PH3 ④还原性:F-->Cl-->Br--
| A.①②④ | B.②③④ | C.①②③ | D.都正确 |
C
试题分析:④错误,还原性应该为Br ->Cl--> F--,因为其单质的氧化性为F2>Cl2>Br2,所以离子的还原性则是倒过来的;①②③正确,故答案为C。
点评:本题综合考查了元素周期律的相关知识点,属于高考考查的重点,本题难度适中。

练习册系列答案
相关题目
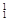 H、
H、 H、
H、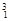 H2、H+、H2互为同位素
H2、H+、H2互为同位素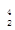 He的最外层电子数为2,所以
He的最外层电子数为2,所以 Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0  Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)