题目内容
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ① | |||||||
二 | ② | ③ | ④ | |||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在标号元素中,最活泼的金属元素是____。最活泼的非金属元素是____。(写元素符号)⑨元素的离子结构示意图是____________________。
(2)①与②形成共价化合物的电子式________________。用电子式表示⑤与⑨形成化合物的形成过程__________________________________________。
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是________。(写元素符号)
(4)⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是____(写分子式);其三种元素的最高价含氧酸的酸性由强到弱的顺序 _________。(写酸的分子式)
(5)写出⑥元素的单质与氢氧化钠反应的离子方程式:____________________。
【答案】 Na F 
![]() Na>Al>Si HCl HClO4> H3PO4> H2SiO3 2Al + 2OH- +2H2O = 2AlO2- + 3H2↑
Na>Al>Si HCl HClO4> H3PO4> H2SiO3 2Al + 2OH- +2H2O = 2AlO2- + 3H2↑
【解析】根据元素在周期表中的位置可知,①为H元素,②为C元素,③为O元素,④为F元素,⑤为Na元素,⑥为Al元素,⑦为Si元素,⑧为P元素,⑨为Cl元素。
(1)根据元素的金属性和非金属性的变化规律,同一周期,从左到右,金属性逐渐减弱,非金属性逐渐增强,同一主族,从上到下,金属性逐渐增强,非金属性逐渐减弱,最活泼的金属元素是钠。最活泼的非金属元素是氟。氯为17号元素,离子结构示意图为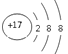 ,故答案为:Na ;F;
,故答案为:Na ;F; ;
;
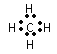
(2)①与②形成共价化合物可以为甲烷,电子式为 。⑤与⑨形成化合物为氯化钠,属于离子化合物,用电子式表示氯化钠的形成过程为
。⑤与⑨形成化合物为氯化钠,属于离子化合物,用电子式表示氯化钠的形成过程为![]() ,故答案为:
,故答案为: ;
; ![]() ;
;
(3)同一周期,从左到右,原子半径逐渐减小,⑤、⑥、⑦三种元素的原子半径由大到小的顺序为Na>Al>Si,故答案为:Na>Al>Si;
(4) 同一周期,从左到右,非金属性逐渐增强,非金属性越强,氢化物越稳定,⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是HCl;非金属性越强,最高价含氧酸的酸性越强,三种元素的最高价含氧酸的酸性由强到弱的顺序为HClO4> H3PO4> H2SiO3,故答案为:HCl;HClO4> H3PO4> H2SiO3;
(5)铝与氢氧化钠反应的离子方程式为2Al + 2OH- +2H2O = 2AlO2- + 3H2↑,故答案为:2Al + 2OH- +2H2O = 2AlO2- + 3H2↑。

【题目】硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,可以通过出现浑浊的快慢来判断反应的快慢程度,下列各组实验中最先出现浑浊的是( )
实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | ||
V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | ||
A | 25 | 5 | 0.1 | 20 | 0.1 |
B | 25 | 5 | 0.2 | 10 | 0.2 |
C | 35 | 5 | 0.1 | 20 | 0.1 |
D | 35 | 5 | 0.2 | 10 | 0.2 |
A. A B. B C. C D. D