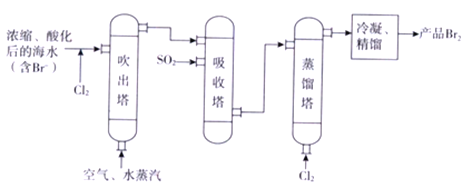
��Ŀ����
����Ŀ��ijѧ����������װ��̽�������백֮��ķ�Ӧ������A��F�ֱ�Ϊ�����������ķ���װ�ã�CΪ��������������백��Ӧ��װ�ã�

��ش��������⣺
��1��װ��F�з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
��2��װ��B��������������________��װ��E��������________��
��3����װ��A����ƿ�ڼ����ĩ״����IJ�����_______________________________��
��4��װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ��д����Ӧ�Ļ�ѧ����ʽ_____________________________________��
����amol�����μӷ�Ӧʱ��ת�Ƶĵ�������Ϊb�������ӵ�����Ϊ________mol-1���ú�a��b�Ĵ���ʽ��ʾ����
��5������F��E��Dװ���Ƶõ�����ͨ�뺬74gCa(OH)2��ʯ�����У������Ƶ�Ư��_______g��
���𰸡�MnO2+4HCl��Ũ���� MnCl2+Cl2��+2H2O ����� ��ȥ�����е��Ȼ��� ����ƿ��ţ���ʢ��ҩƿ��ҩ��ֽ������ƿ�ף��ٽ���ƿ���� 8NH3+3Cl2=6NH4Cl+N2 ![]() 127
127
��������
ʵ��Ŀ����̽��������NH3�ķ�Ӧ��װ��A�Ʊ�������װ��B���ﰱ����װ��CΪNH3��Cl2��Ӧ��װ�ã�װ��F�Ʊ�������װ��E��ȥ������HCl��װ��DΪ����������
��1��װ��F�Ʊ��������䷴Ӧ����ʽΪMnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O��
MnCl2��Cl2����2H2O��
��2������װ��B�������ص㣬����BΪ(����)����ܣ�װ��F�Ʊ���Cl2�л���HCl��H2O(g)��HCl����NH3��Ӧ�������ȥ��װ��E�������dz�ȥ�����л��е�HCl��
��3�������ĩ����IJ����ǽ���ƿ��ţ���ʢ��ҩƿ��ҩ��ֽ������ƿ�ף��ٽ���ƿ����
��4�����������������ԣ���NH3������N2��װ��C�г��ְ��̣�����ΪNH4Cl����Ӧ����ʽΪ8NH3��3Cl2=6NH4Cl��N2��amol��������÷�Ӧ��ת�Ƶ������ʵ���Ϊ2amol������ת�Ƶ�������Ϊb��������n=N/NA����˰����ӵ�����Ϊb/2amol��1��
��5��Cl2��Ca(OH)2�����ķ�Ӧʽ2Cl2��2Ca(OH)2=CaCl2��Ca(ClO)2��2H2O��Ư��ΪCaCl2��Ca(ClO)2����74gCa(OH)2�����ʵ���Ϊ74g/74g��mol��1=1mol,�����ݷ�Ӧ����ʽ�����CaCl2��Ca(ClO)2�������ֱ�Ϊ111/2g��143/2g����Ư�۵�����Ϊ(111/2g��143/2g)=127g��

 ��У����ϵ�д�
��У����ϵ�д�