题目内容
【题目】已知烃被酸性KMn04溶液氧化时,碳碳双键或叁键将断裂生成-![]() -或—COOH。某烃的分子式为某烃的分子式为C11H20, lmol该烃在催化剂作用下可以吸收2mol H2;用热的酸性KMn04溶液氧化,得到下列三种有机物:CH3-CO-CH2-CH3 , CH3-CO-CH3,HOOC-CH2CH2—COOH由此推断写出该烃可能的结构简式是_________________ 。
-或—COOH。某烃的分子式为某烃的分子式为C11H20, lmol该烃在催化剂作用下可以吸收2mol H2;用热的酸性KMn04溶液氧化,得到下列三种有机物:CH3-CO-CH2-CH3 , CH3-CO-CH3,HOOC-CH2CH2—COOH由此推断写出该烃可能的结构简式是_________________ 。
【答案】![]()
【解析】
1mol该烃在催化剂作用下可以吸收2mol H2,则含2个C=C或1个C≡C;酸性KMnO4溶液氧化,得到CH3-CO-CH2-CH3 CH3-CO-CH3和HOOC-CH2CH2—COOH三者的混合物,则含2个C=C,分子式为C11H20的结构简式为![]() ,故答案为:
,故答案为:![]() 。
。

【题目】天空不是垃圾场,污染气体不能随便排,研究大气污染气体的处理方法具有重要意义。
(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) △H=-a kJ·mol-1 (a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-b kJ·mol-1 (b>0)
若用标准状况下3.36LNO2氧化CO至CO2(NO2完全反应)的整个过程中放出的热量为_________ kJ(用含有a和b的代数式表示)。
(2) 已知下列反应的反应热:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) △H=-870.3kJ/mo1
②C(s)+O2(g) =CO2(g) ΔH=-393.5kJ/mo1
③2C(s)+2H2(g)+O2(g) =CH3COOH(1) ΔH=-488.3kJ/mo1
请写出H2燃烧热的热化学方程式______________________________________。
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:
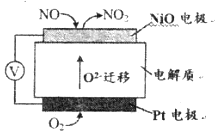
①NiO电极上发生的是_______________反应(填“氧化”或“还原”)。
②Pt电极上的电极反应式为_______________。
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO ![]() 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
实验 编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.20×10-3 | B | 124 |
Ⅲ | 350 | A | 5.80×10-3 | 82 |
①请把表中数据补充完整:A_______________;B_______________。
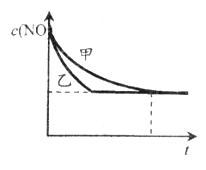
②能验证温度对化学反应速率影响规律的是实验_______________(填实验序号)。
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如下图所示,其中表示实验Ⅱ的是曲线_________(填“甲”或“乙”)。