题目内容
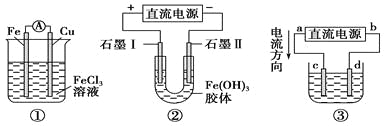
【题目】按下图装置进行实验,并回答下列问题
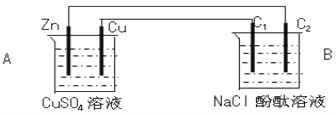
(1)锌极为__________极,电极反应式为__________________________________
(2)石墨棒C1为______极,电极反应式为________________________________,石墨棒C2附近发生的实验现象为__________________________________
(3)当C2极析出224mL气体(标准状态)时,此时装置B中OH-的物质的量为________mol。
【答案】 负极 Zn-2e- = Zn2+ 阳极 2Cl--2e- =Cl2↑ 有气体产生,溶液变红色 0.02
【解析】试题分析:根据图示,A装置中两个电极不同、B装置中两个电极相同,所以A是原电池,锌是负极、铜是正极,电池总反应是![]() ;B是电解池,C1与原电池正极相连,C1是阳极;C2与原电池负极相连,C2是阴极;用惰性电极电解硫酸铜溶液,电解池的总反应是
;B是电解池,C1与原电池正极相连,C1是阳极;C2与原电池负极相连,C2是阴极;用惰性电极电解硫酸铜溶液,电解池的总反应是![]() 。
。
解析:根据以上分析,(1)锌的活泼性大于铜,锌极为负极极,负极失电子发生氧化反应,电极反应式为Zn-2e- = Zn2+;
(2)C1与原电池正极相连,C1是阳极,阳极失电子发生氧化反应,电极反应式为2Cl--2e- =Cl2↑,石墨棒C2是阴极,阴极发生还原反应,电极反应是![]() ,所以现象是有气体产生,溶液变红色;
,所以现象是有气体产生,溶液变红色;
(3)C2极的电极反应式![]() ,C2极析出224mL氢气(标准状态)时,生成氢氧根离子0.02mol,此时装置B中OH-的物质的量为0.02mol。
,C2极析出224mL氢气(标准状态)时,生成氢氧根离子0.02mol,此时装置B中OH-的物质的量为0.02mol。

【题目】Ⅰ.实验是化学研究的一种重要手段,现有下图所示A-G七种仪器,请根据要求填空。
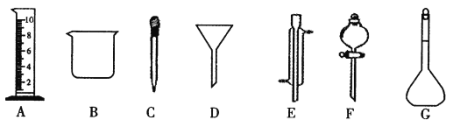
(1)写出仪器名称:E_____________,F_____________。
(2)上述仪器中实验之前需检查装置是否会漏水的是______________(填仪对应字母)。
(3)下列实验操作中用到仪器D的是_________(选填下列选项的编号字母 )。
A.分离水和CCl4的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200 mL1 mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
应称取Na2CO3的质量______(g) | 应选用容量瓶的规格 _______(mL) | 除容量瓶外还需要的其它玻璃仪器是上图中的量筒、烧杯、_____(填仪器名称)及玻璃棒 |
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只能用一次)______________。
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(3)若出现如下情况,对所配溶液浓度将有何影响 (填“偏高”、“偏低”或“无影响”)?
没有进行C操作________;配制溶液时,容量瓶未干燥_________;定容时俯视刻度线_________。
(4)在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是_______________。