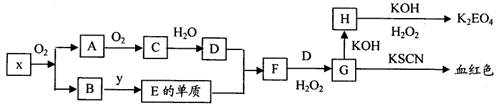
题目内容
为测定某一铁矿石样品中的铁元素的质量分数,取3.702 g该铁矿石(铁以Fe2O3形式存在,其余物质不含铁)溶于浓热盐酸中,稀释至250 mL,从中取出25 mL溶液,作如下处理:加入过量的氨水,使铁以氢氧化铁的形式沉淀,将沉淀过滤,洗净并灼烧,使之完全转化为氧化铁。有关实验数据:坩埚质量:15.286 1 g;第一次灼烧后坩埚和固体的质量:15.620 9 g;第二次灼烧后坩埚和固体的质量:15.620 5 g;第三次灼烧后坩埚和固体的质量:15.620 5 g,则铁矿石中的铁元素的质量分数为( )
| A.63.2% | B.90.3% | C.6.32% | D.34.4% |
A
此题主要考查实验数据分析及计算能力。经分析第一次灼烧后坩埚和固体的质量:15.620 9 g不能用,所以氧化铁的质量=15.620 5 g-15.286 1 g=0.334 4 g,所以铁矿石样品中Fe2O3的质量=3.344 g,铁元素的质量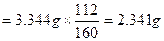 ,铁元素的质量分数
,铁元素的质量分数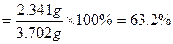 。
。
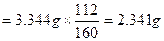 ,铁元素的质量分数
,铁元素的质量分数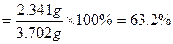 。
。
练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目