题目内容
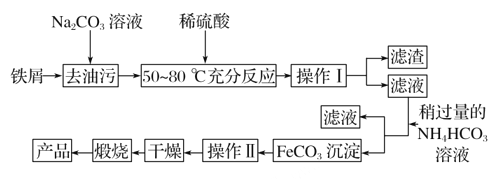
【题目】现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下:

有关说法错误的是
A.反应Ⅰ原理为CO2 + NH3 + NaCl + H2O =NaHCO3↓ + NH4Cl
B.向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3
C.反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱
D.CO2的结构式为O=C=O,其中碳氧原子均满足8电子稳定结构
【答案】B
【解析】
试题分析:饱和氯酸钠中通入氨气和二氧化碳生成碳酸氢钠沉淀和氯化铵,碳酸氢钠受热分解生成碳酸钠和二氧化碳和水。A、由发生的反应可知反应I原理为CO2 + NH3 + NaCl + H2O =NaHCO3↓ + NH4Cl,故A正确;B、氯化钠饱和溶液中二氧化碳的浓度较小,所以应该向饱和氯化钠溶液中先通入足量的氨气,,后通入足量的二氧化碳,错误,选B;C、根据反应生成的沉淀,经过过量洗涤,煅烧克得到纯碱,正确,不选C;D、在二氧化碳分子中碳原子核氧原子之间形成两对共用电子对,所以结构式为O=C=O,碳原子核氧原子都满足8电子结构,正确,不选D。

【题目】已知反应2CH3OH(g)![]() CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/mol·L-1 | 0.44 | 0.6 | 0.6 |
下列叙述中正确的是 ( )
A. 该反应的平衡常数表达式为K=[c(CH3OCH3)×c(H2O)]/c(CH3OH)
B. 此时正、逆反应速率的大小:v正<v逆
C. 若经10 min后反应达到平衡,此时c(CH3OH)=0.04 mol·L-1
D. 0~10min内平均反应速率v(CH3OH)=1.6 mol·(L·min)-1