题目内容
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
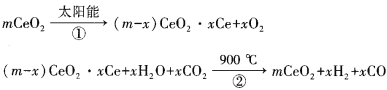
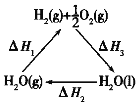
下列说法不正确的是
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
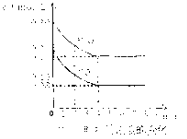
C.图中△H1=△H2+△H3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32—+2H2O
【答案】C
【解析】
试题分析:A.通过太阳能实现总反应:H2O+CO2→H2+CO+O2,CeO2没有消耗,CeO2是光催化剂,故A正确;B.该过程中在太阳能作用下将H2O、CO2转变为H2、CO,所以把太阳能转变成化学能,故B正确;C.由右图可知,根据盖斯定律,应该是:-△H1=△H2+△H3;故C错误;D.CO在负极失电子生成CO2,在碱性条件下再与OH-生成CO32-,故负极反应式正确;故D正确;故选C。

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目