题目内容
两种金属的混合物粉末15 g,与足量的盐酸反应时,恰好得到11.2L标准状况下的氢气,下列各组金属能构成符合上述条件的混合物的是
| A.Na和Ag | B.Cu和Zn |
| C.Al和Fe | D.Mg和Al |
C
用平均值法:11.2 L标准状况下氢气的物质的量为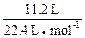 即0.5mol,得到电子为:0.5mol×2=1mol,即金属失去1mol电子的平均质量为15g,必有一物质失去1mol电子其质量大于15g,而另一种物质失去1mol电子其质量小于15g.A项:Na失1mol电子其质量为23g,Ag不反应可看成大于15g,所以A不正确.B项:Zn:
即0.5mol,得到电子为:0.5mol×2=1mol,即金属失去1mol电子的平均质量为15g,必有一物质失去1mol电子其质量大于15g,而另一种物质失去1mol电子其质量小于15g.A项:Na失1mol电子其质量为23g,Ag不反应可看成大于15g,所以A不正确.B项:Zn: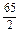 =32.5g、Cu看成大于15g.Cu、Zn均大于15g,故不符合;C项:Al:
=32.5g、Cu看成大于15g.Cu、Zn均大于15g,故不符合;C项:Al: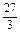 =9g、Fe:
=9g、Fe: =28g,C符合.D项:Mg:
=28g,C符合.D项:Mg: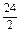 =12g、Al:9g,都小于15g,故D不符合.
=12g、Al:9g,都小于15g,故D不符合.
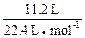 即0.5mol,得到电子为:0.5mol×2=1mol,即金属失去1mol电子的平均质量为15g,必有一物质失去1mol电子其质量大于15g,而另一种物质失去1mol电子其质量小于15g.A项:Na失1mol电子其质量为23g,Ag不反应可看成大于15g,所以A不正确.B项:Zn:
即0.5mol,得到电子为:0.5mol×2=1mol,即金属失去1mol电子的平均质量为15g,必有一物质失去1mol电子其质量大于15g,而另一种物质失去1mol电子其质量小于15g.A项:Na失1mol电子其质量为23g,Ag不反应可看成大于15g,所以A不正确.B项:Zn: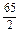 =32.5g、Cu看成大于15g.Cu、Zn均大于15g,故不符合;C项:Al:
=32.5g、Cu看成大于15g.Cu、Zn均大于15g,故不符合;C项:Al: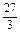 =9g、Fe:
=9g、Fe: =28g,C符合.D项:Mg:
=28g,C符合.D项:Mg: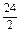 =12g、Al:9g,都小于15g,故D不符合.
=12g、Al:9g,都小于15g,故D不符合.
练习册系列答案
相关题目
