题目内容
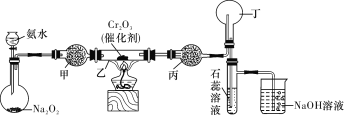
【题目】某化学小组的同学模拟工业制硝酸设计了如下图所示的装置。已知:
CaCl2+nH2O→CaCl2·nH2O;CaCl2+8NH3→[Ca(NH3)8]Cl2,根据题意完成下列填空:
(1)分液漏斗中氨水的浓度为9.0 mol/L。现用质量分数为35%、密度为0.88 g/cm3的氨水配制9.0 mol/L的氨水100 mL,需要的定量仪器有 (选填编号)。
a.100 mL容量瓶 b.10 mL量筒 c.50 mL量筒 d.电子天平
(2)受热时,乙中反应的化学方程式为 。
(3)实验开始先加热催化剂,当催化剂达红热时再打开分液漏斗活塞并移走酒精灯,可观察到的现象有 。
(4)干燥管甲的作用是 ;丙中盛放的药品为 (选填下列编号),其目的是 。
a.浓H2SO4 b.无水CaCl2 c.碱石灰 d.无水CuSO4
(5)丁中除了NO之外,还可能存在的气体有 (填写化学式)。烧杯中发生反应的化学方程式 。
【答案】(1)ac
(2)4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
(3)乙中Cr2O3仍能保持红热状态;丁的烧瓶中气体由无色转化为红棕色;试管里的石蕊试液由紫色变为红色
(4)干燥氧气和氨气的混合气体;b;吸收水及多余NH3
(5)N2、O2、NO2(N2O4);2NO2+2NaOH===NaNO2+NaNO3+H2O、NO+NO2+2NaOH===2NaNO2+H2O
【解析】
试题分析:(1)浓氨水的浓度为c=![]() =
=![]() =18.1 mol/L,由于浓氨水稀释前后溶质的物质的量不变,设浓氨水的体积为V,则18.1 mol/L×V=9.0 mol/L×0.1 L,V=0.0497 L=49.7 mL。因此整个过程中需要的定量容器有100 mL的容量瓶和50 mL的量筒。故答案为:ac;
=18.1 mol/L,由于浓氨水稀释前后溶质的物质的量不变,设浓氨水的体积为V,则18.1 mol/L×V=9.0 mol/L×0.1 L,V=0.0497 L=49.7 mL。因此整个过程中需要的定量容器有100 mL的容量瓶和50 mL的量筒。故答案为:ac;
(2)受热时,乙中的氨气和氧气在催化剂的作用下,发生氧化还原反应,生成NO和H2O,从而写出化学方程式为:4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。
(3)实验开始先加热催化剂,当催化剂达红热时再打开分液漏斗活塞并移走酒精灯,催化剂可以继续保持红热,原因是反应放热;NO在丁的烧瓶中与氧气反应生成红棕色的NO2,NO2溶于水产生硝酸,硝酸能够使紫色石蕊试液变红色。
(4)干燥管甲的作用是干燥氧气与氨气的混合气体;丙为盛装固体的干燥管,其作用是吸收未反应的氨气并干燥NO,因此应该选用无水CaCl2。
(5)由于烧瓶丁中有空气,NO能与空气中的氧气反应生成NO2,NO2会转化成N2O4,所以丁中除了NO之外,还可能存在的气体有N2、O2、NO2 (N2O4);最终氢氧化钠溶液的作用是尾气处理,吸收NO和NO2,方程式2NO2+2NaOH===NaNO2+NaNO3+H2O,NO+NO2+2NaOH===2NaNO2+H2O。

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H1-△H2=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取降温措施