题目内容
(10分)向200 mL ,某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7。
(1)此时溶液的溶质如果是单一成分,可能是____________________;如果是多种成分,可能是__________________________。
(2)在上述所得溶液中,逐滴缓慢滴加2 mol·L-1的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示:
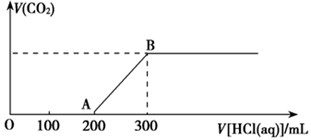
①加入盐酸200 mL之前,无气体产生,写出OA段发生反应的离子方程式______________________________________________________。
②B点时,反应所得溶液中溶质的物质的量浓度是__________ (溶液体积的变化忽略不计)。
(1)此时溶液的溶质如果是单一成分,可能是____________________;如果是多种成分,可能是__________________________。
(2)在上述所得溶液中,逐滴缓慢滴加2 mol·L-1的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示:

①加入盐酸200 mL之前,无气体产生,写出OA段发生反应的离子方程式______________________________________________________。
②B点时,反应所得溶液中溶质的物质的量浓度是__________ (溶液体积的变化忽略不计)。
(1)Na2CO3或NaHCO3(2分)NaOH和Na2CO3或Na2CO3和NaHCO3(2分)
(2)①OH-+H+===H2O(2分),CO+H+===HCO(2分)
②1.2 mol·L-1(2分,不写单位不得分)
(2)①OH-+H+===H2O(2分),CO+H+===HCO(2分)
②1.2 mol·L-1(2分,不写单位不得分)
(1)CO2和氢氧化钠溶液反应,可以生成碳酸钠,也可以生成碳酸氢钠。所以如果是单一成分,则可以是Na2CO3或NaHCO3;如果是多种成分,则可以是NaOH和Na2CO3或Na2CO3和NaHCO3。
(2)由于碳酸钠和盐酸反应是分步进行的,方程式为Na2CO3+HCl=NaCl=NaHCO3、NaHCO3+HCl=NaCl+H2O+CO2↑。根据图像可知,生成CO2消耗盐酸的物质的量小于前面消耗的,这说明溶液中的溶质是氢氧化钠和碳酸钠。所以O到A点发生反应的离子方程式是OH- + H+ = H2O、CO32-+ H+ = HCO3-。
(3)根据图像可知最终溶液中生成的是氯化钠。根据原子守恒可知,氯化钠是0.3L×2mol/L=0.6mol,所以再根据原子守恒可知,氢氧化钠元也是0.6mol,则浓度是0.6mol÷0.5L=1.2mol/L。
(2)由于碳酸钠和盐酸反应是分步进行的,方程式为Na2CO3+HCl=NaCl=NaHCO3、NaHCO3+HCl=NaCl+H2O+CO2↑。根据图像可知,生成CO2消耗盐酸的物质的量小于前面消耗的,这说明溶液中的溶质是氢氧化钠和碳酸钠。所以O到A点发生反应的离子方程式是OH- + H+ = H2O、CO32-+ H+ = HCO3-。
(3)根据图像可知最终溶液中生成的是氯化钠。根据原子守恒可知,氯化钠是0.3L×2mol/L=0.6mol,所以再根据原子守恒可知,氢氧化钠元也是0.6mol,则浓度是0.6mol÷0.5L=1.2mol/L。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
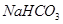 和
和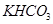 组成的混合物18.400 g,与100 mL盐酸反应。(题中涉及的气体体积均为标准状况下,填空时可以用带字母的式子表示。)
组成的混合物18.400 g,与100 mL盐酸反应。(题中涉及的气体体积均为标准状况下,填空时可以用带字母的式子表示。) 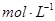 。
。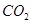 的体积为 L。
的体积为 L。