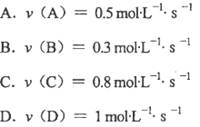题目内容
在 反应中,表示该反应速率最快的是( )。
反应中,表示该反应速率最快的是( )。
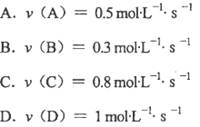
 反应中,表示该反应速率最快的是( )。
反应中,表示该反应速率最快的是( )。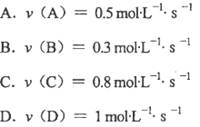
B
试题分析:根据在同一反应中化学反应速率之比等于化学方程式中化学计量数之比,将上述4个答案都转化成以反应物A表示的形式,则B、v(A)=0.6mol·L-1·s-1,C、v(A)= 1.6/3 mol·L-1·s-1,D、v(A)=0.5 mol·L-1·s-1,所以B选项是数值最大,答案选B。

练习册系列答案
相关题目
题目内容
 反应中,表示该反应速率最快的是( )。
反应中,表示该反应速率最快的是( )。