题目内容
若20 g密度为d g/cm3的硝酸钙溶液里含1 g Ca2+,则NO3-的浓度是
| A.d/400 mol·L-1 | B.20/d mol·L-1 | C.2.5d mol·L-1 | D.1.25d mol·L-1 |
C
试题分析:20克密度为d克/厘米3的硝酸钙溶液的体积为20g÷dg/cm3=(20/d)cm3=(20/d)×10-3L,
1克Ca2+的物质的量为1g÷40g/mol=0.025mol,
则Ca2+的物质的量浓度为0.025mol÷(20/d)×10-3L=1.25dmol/L,
由硝酸钙的化学式Ca(NO3)2,
则NO3-离子的浓度为1.25dmol/L×2=2.5mol/L,
故选C。
点评:本题考查物质的量浓度的计算,明确钙离子的物质的量的计算是解答的关键,钙离子的质量与钙原子的质量可近似相等,忽略电子的质量来分析解答。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
 2NaAlO2+3H2。该反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)
2NaAlO2+3H2。该反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)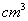 )配制100mL 1 mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,配制中使用仪器的先后顺序排列正确的是( )
)配制100mL 1 mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,配制中使用仪器的先后顺序排列正确的是( )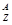 X和足量的稀H2SO4反应,生成6.02×1022个
X和足量的稀H2SO4反应,生成6.02×1022个