题目内容
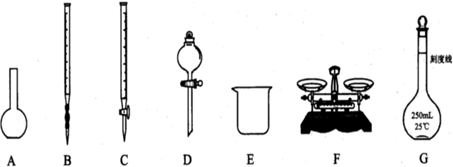
准确量取25.00mL高锰酸钾溶液,可选用的仪器是( )
分析:准确量取25.00mL高锰酸钾溶液,需要用精密量具,精确到0.1,估读到0.01,所以学过的量具,滴定管、移液管是能精确计量的仪器;注意高锰酸钾溶液的强氧化性;
解答:解:量筒是不能精确地计量的仪器,滴定管、移液管是能精确计量的仪器.准确量取25.00mL溶液,应用25ml的滴定管,50mL滴定管可以量取.又因为碱式滴定管的下端有一段橡皮管,高锰酸钾具有强腐蚀性,量取高锰酸钾溶液要用酸式滴定管;
故选BC.
故选BC.
点评:本题考查了化学中常见的准确量取液体的仪器和粗略量取的仪器的使用方法和注意问题.

练习册系列答案
相关题目
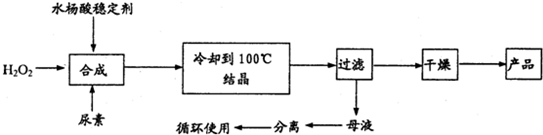
(12分)①制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
②用NaOH测定滤液的浓度:准确称量1.000gNaOH固体质量,配制成250mL溶液,准确量取25.00mL溶液装在碱式滴定管,滴加2滴酚酞作指示剂。把滤液装在酸式滴定管中,调节液面排除气泡后,滤液的凹液面刚好在“0”刻度,滴定NaOH溶液,达到终点记录读数。实验重复3次。记录见下表。
|
滴定次数 |
NaOH溶液体积/mL |
滴定消耗滤液体积/mL[来源: |
|
1 |
25.00 |
20.02 |
|
2 |
25.00 |
17.10 |
|
3 |
25.00 |
19.98 |
请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为_______________________________。
(2) 配制成250mL溶液使用的量具是 ,指示剂还可用____________;
(3) 滴定终点的现象是_______________________。
(4) 滤液中溶质的物质的量浓度为_____________。
(5) 若在滴定终点读取滴定管刻度时,俯视标准液液面,使对测定结果________。 (填“偏高”、“偏低”或“无影响”)