题目内容
13. 如图为A(气)+B(气)?nC(气)+Q在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线.下列有关叙述正确的是( )
如图为A(气)+B(气)?nC(气)+Q在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线.下列有关叙述正确的是( )| A. | 若其它条件相同,a比b的温度高 | |
| B. | a表示有催化剂,b表示无催化剂 | |
| C. | 若n=2,其它条件相同,a比b的压强大 | |
| D. | 反应由逆反应开始 |
分析 A、温度高,到达平衡时间短,再根据升温,平衡移动分析;
B、加入催化剂同等程度增大正逆反应速率,平衡不移动;
C、压强越大到达平衡时间短,平衡时C的百分含量(C%)越小,可知正反应为气体物质的量增大的反应;
D、从C的百分含量的变化判断.
解答 解:A、a到达平衡时间短,所以a温度高,升温平衡时C的百分含量(C%)减小,平衡逆向移动,所以△H<0,故A正确;
B、加入催化剂同等程度增大正逆反应速率,平衡不移动,则a、b到达平衡时C的百分含量相同,故B错误;
C、a到达平衡时间短,所以a压强高,压强越大,平衡时C的百分含量(C%)越小,可知正反应为气体物质的量增大的反应,所以n>2,故C错误;
D、C的百分含量从零开始逐渐增大,所以反应从正反应开始,故D错误;
故选A.
点评 本题考查了外界条件对速率和平衡的影响,难度不大,明确“先拐先平数值大”是解本题的关键,注意把握温度、压强、催化剂对速率及平衡的影响.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
3. 常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为离子晶体;
(2)冰比硫化氢热稳定性高的原因是O-H键的键长小于H-S键的键长,硫化氢的分子空间构型为V形;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
则X、Y、Z的电负性从大到小的顺序为Al、Mg、Na(用元素符号表示),元素Y第一电离能大于X的原因是因为元素Mg价电子排布式为3s2完全充满状态,比Al稳定;
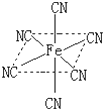
(4)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损.铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成配合物黄血盐,配离子结构如图.
①写出铁元素基态原子价电子排布式3d64s2;
②已知CN-与 N2结构相似,1molCN-中π键数目为2NA;
③写出沉淀溶解的化学方程式Fe(CN)2+4KCN=K4[Fe(CN)6].
 常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:(1)“氯盐类”融雪剂主要成分的晶体类型为离子晶体;
(2)冰比硫化氢热稳定性高的原因是O-H键的键长小于H-S键的键长,硫化氢的分子空间构型为V形;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(4)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损.铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成配合物黄血盐,配离子结构如图.
①写出铁元素基态原子价电子排布式3d64s2;
②已知CN-与 N2结构相似,1molCN-中π键数目为2NA;
③写出沉淀溶解的化学方程式Fe(CN)2+4KCN=K4[Fe(CN)6].
4.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列六步操作,下列各组操作顺序合理的是( )
①过滤,
②加稍过量的NaOH溶液,
③向滤液中加适量盐酸,
④加稍过量的Na2CO3溶液,
⑤加稍过量的BaCl2溶液,
⑥将滤液蒸发结晶.
①过滤,
②加稍过量的NaOH溶液,
③向滤液中加适量盐酸,
④加稍过量的Na2CO3溶液,
⑤加稍过量的BaCl2溶液,
⑥将滤液蒸发结晶.
| A. | ②④⑤①③⑥ | B. | ⑤②④①③⑥ | C. | ④②⑤①③⑥ | D. | ②⑤④③①⑥ |
1.下列实验不能达到目的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持50-60℃反应生成硝基苯 | |
| B. | 用水鉴别己烷、四氯化碳、酒精三种无色液体 | |
| C. | 将苯和溴水混合制取溴苯 | |
| D. | 可用酸性高锰酸钾溶液鉴别甲烷和乙烯 |
3.下列有机物不会发生水解反应的是( )
| A. | 脂肪 | B. | 蛋白质 | C. | 葡萄糖 | D. | 纤维素 |

 .B存在同素异形现象,其中常用作消毒剂的是O3.(填化学式)
.B存在同素异形现象,其中常用作消毒剂的是O3.(填化学式) .
.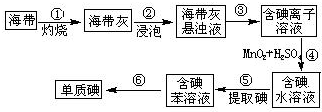 碘在工农业生产和日常生活中有重要用途.
碘在工农业生产和日常生活中有重要用途.