题目内容
【题目】已知2X2(g)+Y2(g)![]() 2Z(g)ΔH=-a kJ·mol-1(a>0),在一个容积固定的密闭容器中加入2 mol X2和1 mol Y2,在500 ℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g)ΔH=-a kJ·mol-1(a>0),在一个容积固定的密闭容器中加入2 mol X2和1 mol Y2,在500 ℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
(1)此反应平衡常数表达式为___________;若将温度降低到300 ℃,则反应平衡常数将________(填“增大”“减少”或“不变”)。
(2)若原容器中只加入2 mol Z,500 ℃充分反应达平衡后,吸收热量c kJ,则Z浓度________W mol·L-1(填“>”“<”或“=”),b、c间的关系为________。(用a、b、c表示)。
(3)能说明反应已达到平衡状态的是________。
a.单位时间内消耗1molY2的同时消耗了2molZ b.容器内的密度保持不变
c. v逆(X2)=2v正(Y2) d.容器内压强保持不变
e.混合气体的平均式量保持不变 f.Y2和X2的转化率相等
(4)若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2 mol X2和1 mol Y2,达到平衡后,Y2的转化率将________(填“变大”“变小”或“不变”)。
【答案】 K=c2(Z)/c(Y2).c2(x2) 增大 = b+c=a acde 变大
【解析】(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,所以2X2(g)+Y2(g)![]() 2Z(g)的平衡常数K=
2Z(g)的平衡常数K=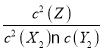 ,该反应ΔH=-a kJ·mol-1(a>0),正反应是放热反应,则降低温度,平衡正向移动,反应平衡常数增大:(2)恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同,故c(Z)=WmolL-1,同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,对于反应2X2(g)+Y2(g)2Z(g)△H=-akJmol-1,则b=n×
,该反应ΔH=-a kJ·mol-1(a>0),正反应是放热反应,则降低温度,平衡正向移动,反应平衡常数增大:(2)恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同,故c(Z)=WmolL-1,同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,对于反应2X2(g)+Y2(g)2Z(g)△H=-akJmol-1,则b=n×![]() ,对于反应2Z(g)2X2(g)+Y2(g)△H=akJmol-1,Z分解的物质的量为(2-n)mol,故c=
,对于反应2Z(g)2X2(g)+Y2(g)△H=akJmol-1,Z分解的物质的量为(2-n)mol,故c= ![]() ×a=1-n×
×a=1-n×![]() ,故a=b+c;(3)平衡的标志是反应的正逆反应速率相同;a.单位时间内消耗1molY2的同时消耗了2mol Z,说明正逆反应速率相同,选项a正确;b. 反应容器体积一定,气体质量守恒,反应过程和平衡状态容器内的密度始终保持不变,选项b错误;c. 依据反应速率之比等于化学方程式的系数之比,v逆(X2)= v正(X2)=2v正(Y2),说明正逆反应速率相等,选项c正确;d.反应是气体压强减小的反应,平衡状态容器内压强保持不变,说明反应达到平衡,选项d正确;e.气体质量恒定,反应未达平衡时物质的量在变化,则平均式量在变化,当混合气体的平均式量保持不变,说明正逆反应速率相等,达到平衡状态,选项e正确;f.Y2和X2都为反应物,只有满足物质的量之比等于化学计量数之比,则转化率始终相等,不能说明达到平衡状态,选项f错误。答案选acde;(4)原平衡随反应进行,压强降低,恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,即向正反应移动,Y2的转化率变大。
,故a=b+c;(3)平衡的标志是反应的正逆反应速率相同;a.单位时间内消耗1molY2的同时消耗了2mol Z,说明正逆反应速率相同,选项a正确;b. 反应容器体积一定,气体质量守恒,反应过程和平衡状态容器内的密度始终保持不变,选项b错误;c. 依据反应速率之比等于化学方程式的系数之比,v逆(X2)= v正(X2)=2v正(Y2),说明正逆反应速率相等,选项c正确;d.反应是气体压强减小的反应,平衡状态容器内压强保持不变,说明反应达到平衡,选项d正确;e.气体质量恒定,反应未达平衡时物质的量在变化,则平均式量在变化,当混合气体的平均式量保持不变,说明正逆反应速率相等,达到平衡状态,选项e正确;f.Y2和X2都为反应物,只有满足物质的量之比等于化学计量数之比,则转化率始终相等,不能说明达到平衡状态,选项f错误。答案选acde;(4)原平衡随反应进行,压强降低,恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,即向正反应移动,Y2的转化率变大。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案