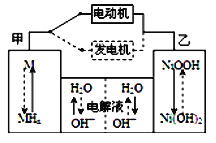
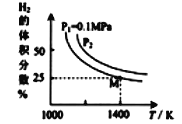
题目内容
【题目】已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19,用0.1molL-1NaOH溶液滴定20mL0.1molL-1H2A溶液的滴定曲线如图所示。下列说法不正确的是
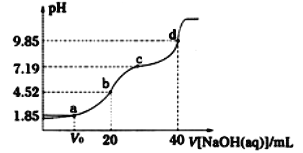
A. c点所得溶液中:c(A2-)=c(HA-)
B. b点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
C. A2-水解平街常数Kh(A2-)=10-7.19
D. a点所得溶液中,V0=10mL
【答案】A
【解析】pKa2=7.19,则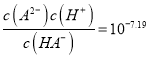 ,c点PH=7.19,
,c点PH=7.19, ![]() ,所以c(A2-)=c(HA-),故A正确;b点是20mL0.1molL-1NaOH溶液与20mL0.1molL-1H2A溶液混合,溶质为NaHA,根据质子守恒c(H2A)+c(H+)=c(A2-)+c(OH-),故B错误;A2-水解平街常数Kh(A2-)
,所以c(A2-)=c(HA-),故A正确;b点是20mL0.1molL-1NaOH溶液与20mL0.1molL-1H2A溶液混合,溶质为NaHA,根据质子守恒c(H2A)+c(H+)=c(A2-)+c(OH-),故B错误;A2-水解平街常数Kh(A2-)![]() =10-6.81,故C错误;若V0=10mL,则溶质为等浓度的H2A、NaHA,H2A电离大于HA-水解,所以c(HA-)>c(H2A),而a点溶液PH=1.85,c(HA-)= c(H2A),故D错误。
=10-6.81,故C错误;若V0=10mL,则溶质为等浓度的H2A、NaHA,H2A电离大于HA-水解,所以c(HA-)>c(H2A),而a点溶液PH=1.85,c(HA-)= c(H2A),故D错误。

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目