题目内容
制备下列气体过程中,净化除杂的有关操作(括号内是杂质)其中正确的是
- A.CO2(CO);气体通过灼热的CuO
- B.C2H4(SO2);气体通过盛有溴水的洗气瓶
- C.NO(NO2);通过水洗干燥后,用向下排空气法收集
- D.NH3(H2O);气体通过浓H2SO4
A
解析:
导解:溴水会吸收C2H4,B不正确;
NO会与O2反应,C不正确;
浓H2SO4吸收NH3,D不反应.
解析:
导解:溴水会吸收C2H4,B不正确;
NO会与O2反应,C不正确;
浓H2SO4吸收NH3,D不反应.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
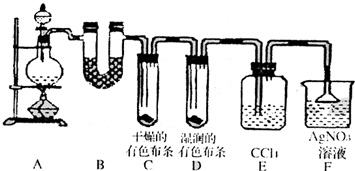 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
