题目内容
16.在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图:
(1)连接上述仪器的正确顺序(填各接口处的字母):E接C;D接A;B接H;G接F.
(2)装置中,饱和食盐水的作用是除去Cl2中的HCl;浓硫酸的作用是除去Cl2中的H2O.
(3)化学实验中检验是否有Cl2产生的常用方法是湿润的淀粉KI试纸变蓝,反应的离子方程式2I-+Cl2═2Cl-+I2.
(4)写出下列反应的化学方程式:
①气体发生装置中进行的反应:4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.②NaOH溶液中发生的反应:2NaOH+Cl2═NaClO+NaCl+H2O.
(5)如果将10mL 12mol•L-1的浓盐酸与足量MnO2充分反应,实际能收集到的氯气在标准状况下的体积将D.
A.≥0.672L B.>0.672L C.≤0.672L D.<0.672L.
分析 (1)气体制备一般经过气体的发生装置,净化、除杂、干燥装置,再经收集装置,尾气处理装置,据此解答;
(2)制备的氯气中含有氯化氢和水蒸气,氯化氢易溶于水,在饱和食盐水中溶解度不大,利用饱和食盐水除去氯化氢,浓硫酸具有吸水性,利用浓硫酸干燥氯气;
(3)氯气具有强的氧化性,能够氧化碘离子生成碘,碘遇到淀粉变蓝;
(4)盐酸与二氧化锰在加热条件下反应生成氯化锰、氯气和水;氯气与氢氧化钠溶液反应生成氯化钠、次氯酸和水;
(5)只有浓盐酸才能与二氧化锰反应生成氯气,稀盐酸不反应.
解答 解:(1)实验室制备氯气用浓盐酸与二氧化锰,各装置连接顺序为:发生装置,除杂装置,收集装置,尾气处理装置,从发生装置里出来的气体含有杂质氯化氢和水,先通过饱和食盐水除去氯化氢,再通过浓硫酸除去水,氯气密度大于空气密度,应用向上排空气法,导气管长进短出,所以正确的连接顺序为:EC D A B H G F;
故答案为:C;D;A;B;H;G;
(2)从发生装置制取的氯气含有氯化氢和水蒸气,用饱和食盐水吸收氯气中的氯化氢,利用浓硫酸干燥氯气;
故答案为:除去Cl2中的HCl;除去Cl2中的H2O(或答干燥Cl2);
(3)氯气具有强的氧化性,与碘化钾反应生成碘和氯化钾,离子方程式:2 I-+Cl2═2 Cl-+I2,碘遇到淀粉变蓝,利用湿润的淀粉碘化钾检验氯气;
故答案为:湿润的淀粉KI试纸变蓝;2I-+Cl2═2 Cl-+I2;
(4)盐酸与二氧化锰在加热条件下反应生成氯化锰、氯气和水,化学方程式:4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
氯气与氢氧化钠溶液反应生成氯化钠、次氯酸和水,化学方程式:2NaOH+Cl2═Na ClO+NaCl+H2O;
故答案为:4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;2NaOH+Cl2═Na ClO+NaCl+H2O;
(5)10mL 12mol•L-1的浓盐酸含有氯化氢物质的量0.12mol,完全反应生成氯气0.03mol,标况下体积为0.672L,但是随着反应进行盐酸浓度降低变为稀盐酸,稀盐酸与二氧化锰不反应,所以实际生成的氯气的体积小于0.672L,
故选:D.
点评 本题考查了氯气的实验室制备和性质的检验,熟悉氯气的性质和制备原理,注意只有浓盐酸与二氧化锰反应,所以当浓盐酸定量时,实际生成氯气的量小于理论产量,题目难度不大.

 口算题天天练系列答案
口算题天天练系列答案| A. | 它与氧气接触即转变为SO3 | |
| B. | 亚硫酸钙能溶解于它的水溶液中 | |
| C. | 它的密度比空气小,且不易液化 | |
| D. | 它的水溶液是酸性,且能被强氧化剂氧化 |
| A. | 对于反应2HI(g)?H2(g)+I2(g),增大平衡体系的压强(压缩体积),可使体系颜色变深 | |
| B. | 实验室常用排饱和食盐水法收集氯气 | |
| C. | 硫酸工业中,加催化剂有利于三氧化硫的生成 | |
| D. | 2SO2+O2$?_{加热}^{催化剂}$2SO3的反应条件不是室温,是500℃左右 |
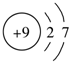
| A. | 一 | B. | 二 | C. | 三 | D. | 四 |
| A. | Al(OH)3→Al2O3 | B. | Al2O3→Al(OH)3 | C. | Al→Al(OH)3 | D. | SiO2→H2SiO3 |
| A. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物 | |
| B. | PM2.5只是地球大气成分中含量很少的组分,对空气质量和能见度等没什么影响 | |
| C. | PM2.5粒径小,富含大量的有毒、有害物质且在大气中的停留时间长、输送距离远 | |
| D. | PM2.5主要来自化石燃料的燃烧(如机动车尾气、燃煤)、挥发性有机物等 |
 K2S
K2S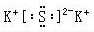 NaOH
NaOH
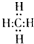 ,分子里各原子的空间分布呈正四面体结构.分子式为C4Hm的烷烃,m值等于10;并写出它的同分异构体的结构简式CH3CH2CH2CH3、(CH3)2CHCH3.
,分子里各原子的空间分布呈正四面体结构.分子式为C4Hm的烷烃,m值等于10;并写出它的同分异构体的结构简式CH3CH2CH2CH3、(CH3)2CHCH3.