题目内容
把0.6 mol 气体X 和0.4 mol 气体Y混合于2.0L的密闭容器中,发生如下反应3X(g)+ Y(g) nZ(g)+2W(g),测得5min末已生成0.2 mol W,又知以Z表示的反应速率为0.01 mol·L-1·min-1,则n值是
nZ(g)+2W(g),测得5min末已生成0.2 mol W,又知以Z表示的反应速率为0.01 mol·L-1·min-1,则n值是
 nZ(g)+2W(g),测得5min末已生成0.2 mol W,又知以Z表示的反应速率为0.01 mol·L-1·min-1,则n值是
nZ(g)+2W(g),测得5min末已生成0.2 mol W,又知以Z表示的反应速率为0.01 mol·L-1·min-1,则n值是| A.1 | B.2 | C.3 | D.4 |
A
分析:根据v=
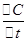 =
= 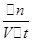 计算A的平均化学反应速率,再根据同一化学反应同一时间段内,各物质的反应速率之比等于计量数之比判断n值.
计算A的平均化学反应速率,再根据同一化学反应同一时间段内,各物质的反应速率之比等于计量数之比判断n值.解:5min内W的平均化学反应速率=
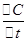 =
= 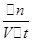 =
= =0.02mol/(L.min),同一化学反应同一时间段内,各物质的反应速率之比等于计量数之比,Z浓度变化表示的平均反应速率为0.01mol/L?min,v(z):v(w)=0.01mol/(L?min):0.02mol/(L.min=n:2),所以n=1,故选A
=0.02mol/(L.min),同一化学反应同一时间段内,各物质的反应速率之比等于计量数之比,Z浓度变化表示的平均反应速率为0.01mol/L?min,v(z):v(w)=0.01mol/(L?min):0.02mol/(L.min=n:2),所以n=1,故选A
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 ,其中气体M、气体N的物质的量随时间变化的曲线如图所示:
,其中气体M、气体N的物质的量随时间变化的曲线如图所示: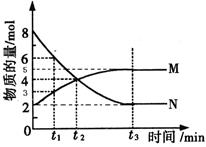
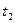 时刻,正逆反应速率大小V正 V逆。
时刻,正逆反应速率大小V正 V逆。
 A.② B.①③ C.②① D.①
A.② B.①③ C.②① D.①