题目内容
【题目】某透明溶液仅含 Na+、F![]() 、B
、B![]() 、Al3+、NO3-、Cl-、SO42-中的 4种离子,所含离子均为 1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。回答下列问题:
、Al3+、NO3-、Cl-、SO42-中的 4种离子,所含离子均为 1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。回答下列问题:
(1)溶液中存在的离子是_________________;
(2)写出溶液中加入过量的稀硫酸反应的离子方程式___________________;
(3)向原溶液中滴加足量NaOH 溶液后,过滤洗涤灼烧,最终得到固体质量为_________g。
【答案】Na+、Fe2+、![]() 、
、![]()
![]() 80
80
【解析】
根据溶液中加入硫酸,有气泡,且溶液中阴离子种类不变,说明溶液发生的反应为亚铁离子被硝酸氧化生成一氧化氮,则溶液中存在亚铁离子和硝酸根离子和硫酸根离子,在根据电荷守恒分析,另外存在的离子只能是钠离子。
(1)溶液中加入硫酸,有气泡产生,且溶液中阴离子种类不变,说明不含有钡离子,有硫酸根离子,气体的产生只能是亚铁离子和硝酸根离子在酸性条件下反应生成的一氧化氮,溶液中4种离子,所含离子均为 1mol,根据电荷守恒分析,另外存在的阳离子为钠离子,故溶液中存在Na+、Fe2+、![]() 、
、![]() ;
;
(2)溶液中加入硫酸,是亚铁离子被硝酸氧化,离子方程式为:![]() ;
;
(3)原溶液中加入过量的氢氧化钠,得到氢氧化亚铁,过滤洗涤灼烧,最终得到固体为氧化铁,根据亚铁离子为1mol分析,氧化铁的物质的量为0.5mol,质量为80g。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
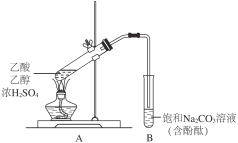
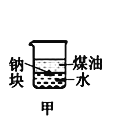
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D