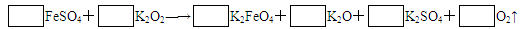题目内容
(8分)用氯气对饮用水消毒已有百年历史。这种消毒方法会使饮用水中的有机物发生氯代反应,生成有机含氯化合物,对人体有害,且氯气本身也是一种有毒气体。世界环保联盟即将全面禁止用氯气对饮用水消毒,建议推广采用广谱性高效消毒剂二氧化氯(ClO2)。目前欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,反应的化学方程式为:
___NaClO3+___HCl===___NaCl+___ClO2↑+___Cl2↑+___H2O。
(1)配平上述化学方程式。
(2)此反应中氧化剂是:__________,在反应中盐酸体现的性质是_________和_________;
(3)在标准状况下有4.48L氯气生成时,转移的电子数为_________mol,被氧化的盐酸的物质的量为________mol。
(4)我国研制成功用氯气氧化亚氯酸钠(在氮气保护下)制得ClO2,表示这一反应的化学方程式是2NaClO2+Cl2==2ClO2↑+2A。已知A物质是一种盐,它的化学式为_________。
这一方法的优点是 。
___NaClO3+___HCl===___NaCl+___ClO2↑+___Cl2↑+___H2O。
(1)配平上述化学方程式。
(2)此反应中氧化剂是:__________,在反应中盐酸体现的性质是_________和_________;
(3)在标准状况下有4.48L氯气生成时,转移的电子数为_________mol,被氧化的盐酸的物质的量为________mol。
(4)我国研制成功用氯气氧化亚氯酸钠(在氮气保护下)制得ClO2,表示这一反应的化学方程式是2NaClO2+Cl2==2ClO2↑+2A。已知A物质是一种盐,它的化学式为_________。
这一方法的优点是 。
(1)2,4,2,2,1,2.(2)NaClO3;还原性、酸性。(3)0.4;0.4。
(4)NaCl;不产生有毒的氯气,减小对环境的污染。
(4)NaCl;不产生有毒的氯气,减小对环境的污染。
考查氧化还原反应的有关判断即计算等。
(1)同一种元素之间发生氧化还原反应时,生成物的价态只能介于中间,且氧化产物的价态不能高于还原产物的价态,即ClO2是还原产物,而氯气是氧化产物,氯酸钾是还原剂,氯化氢是还原剂,所以根据电子的得失守恒可知,配平后的化学计量数依次是2,4,2,2,1,2。
(2)氯酸钾中氯元素的化合价降低,所以氯酸钾是氧化剂;盐酸中氯元素的化合价升高,所以氯化氢是还原剂。又因为还生成氯化钾,所以盐酸还起酸性的作用。
(3)标准状况下,4.48L氯气是0.2mol,则转移电子的物质的量是0.2mol×2=0.4mol,所以被氧化的盐酸就是0.4mol。
(4)根据原子守恒可知,A应该是氯化钠。根据方程式可知,该方法的优点是在反应中不能产生有毒的气体氯气。
(1)同一种元素之间发生氧化还原反应时,生成物的价态只能介于中间,且氧化产物的价态不能高于还原产物的价态,即ClO2是还原产物,而氯气是氧化产物,氯酸钾是还原剂,氯化氢是还原剂,所以根据电子的得失守恒可知,配平后的化学计量数依次是2,4,2,2,1,2。
(2)氯酸钾中氯元素的化合价降低,所以氯酸钾是氧化剂;盐酸中氯元素的化合价升高,所以氯化氢是还原剂。又因为还生成氯化钾,所以盐酸还起酸性的作用。
(3)标准状况下,4.48L氯气是0.2mol,则转移电子的物质的量是0.2mol×2=0.4mol,所以被氧化的盐酸就是0.4mol。
(4)根据原子守恒可知,A应该是氯化钠。根据方程式可知,该方法的优点是在反应中不能产生有毒的气体氯气。

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
 TiO2+H2O ④TiO2+2C+2Cl2
TiO2+H2O ④TiO2+2C+2Cl2