题目内容
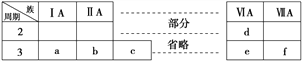
【题目】下表是元素周期表的一部分,表中字母分别表示一种元素。请回答下列问题:

(1)a的一种核素核内有一个质子、一个中子。该核素的符号为______。
(2) 写出元素j在周期表中的位置____________。已知n原子的最外层有两个电子,画出其原子的结构示意图____________。
(3)a、d、f、g、m 五种元素的原子半径由小到大的顺序为________(用元素符号表示)。
(4) c、d、j、l四种元素最高价氧化物对应的水化物的酸性由强到弱的顺序为______(用化学式表示)。
(5)上述元素形成的氢化物中最稳定的是_____(填写名称,下同),溶于水显碱性的是_____。
(6)e、k 两种元素得电子能力强的是_____ (用元素符号表示),用化学方程式证明结论_____ 。
(7)元素a、e 形成的原子个数1:1的化合物的分子式为_____,所含化学键的类型为______。
【答案】 ![]() 第三周期IVA族
第三周期IVA族  H<F<N<Na<K HClO4>HNO3>H2CO3>H4SiO4(H2SiO3) 氟化氢 氨气 O 2H2S+O2=2S+2H2O H2O2 共价键或极性键、非极性键
H<F<N<Na<K HClO4>HNO3>H2CO3>H4SiO4(H2SiO3) 氟化氢 氨气 O 2H2S+O2=2S+2H2O H2O2 共价键或极性键、非极性键
【解析】根据元素所在周期表中的位置可知a为H元素,b为Li元素,c为C元素,d为N元素,e为O元素,f为F元素,g为Na元素,h为Mg元素,i为Al元素,j为Si元素,k为S元素,l为Cl元素,m为K元素,n为Fe元素。(1)a为H元素,它的一种核素核内有一个质子、一个中子。该核素的符号为![]() ;(2)元素j为Si元素,在周期表中的位置第三周期IVA族。已知n原子的最外层有两个电子,其原子的结构示意图
;(2)元素j为Si元素,在周期表中的位置第三周期IVA族。已知n原子的最外层有两个电子,其原子的结构示意图 ;(3)同周期元素从左到右原子半径依次减小,同主族元素原子半径从上到下依次增大,故a、d、f、g、m五种元素的原子半径由小到大的顺序为H<F<N<Na<K;(4)元素非金属性越强,其最高价氧化物的水化物的酸性越强,则c、d、j、l四种元素最高价氧化物对应的水化物的酸性由强到弱的顺序为HClO4>HNO3>H2CO3>H4SiO4(H2SiO3);(5)元素非金属性越强,氢化物越稳定的是,故氢化物最稳定的是氟化氢,氢化物溶于水显碱性的是氨气;(6)同主族从上而下非金属性减弱,元素得电子能力减弱,故e、k两种元素得电子能力强的是O,用化学方程式证明结论2H2S+O2=2S+2H2O;(7)元素a、e形成的原子个数1:1的化合物的分子式为H2O2,所含化学键的类型为共价键或极性键、非极性键。
;(3)同周期元素从左到右原子半径依次减小,同主族元素原子半径从上到下依次增大,故a、d、f、g、m五种元素的原子半径由小到大的顺序为H<F<N<Na<K;(4)元素非金属性越强,其最高价氧化物的水化物的酸性越强,则c、d、j、l四种元素最高价氧化物对应的水化物的酸性由强到弱的顺序为HClO4>HNO3>H2CO3>H4SiO4(H2SiO3);(5)元素非金属性越强,氢化物越稳定的是,故氢化物最稳定的是氟化氢,氢化物溶于水显碱性的是氨气;(6)同主族从上而下非金属性减弱,元素得电子能力减弱,故e、k两种元素得电子能力强的是O,用化学方程式证明结论2H2S+O2=2S+2H2O;(7)元素a、e形成的原子个数1:1的化合物的分子式为H2O2,所含化学键的类型为共价键或极性键、非极性键。