题目内容
FeCl3+3NH4SCN
 Fe(SCN)3+3NH4Cl
Fe(SCN)3+3NH4Cl所得溶液显红色,改变下列条件,能使溶液颜色变浅的是
| A.向溶液中加入少量KCl晶体 |
| B.向溶液中加入少量的水 |
| C.向溶液中加入少量无水硫酸铜,变蓝后立即取出 |
| D.向溶液中滴加2滴1 mol·L-1的FeCl3(aq) |
B
从反应实质来看,溶液中存在的化学平衡是:
Fe3++3SCN- Fe(SCN)3
Fe(SCN)3
等系列反应。可见加入 KCl 晶体,对此平衡无影响;但加入 2 滴 1 mol·L-1的 FeCl3(aq),使溶液中 Fe3+浓度增大,平衡则向正反应方向移动,溶液颜色变深。A、D 项皆不可选。
对于 B、C 选项,因平衡体系中的水量发生了改变,导致溶液中所有溶质的浓度或同等程度地增大,或同等程度地减小;若要判断平衡移动的方向,从浓度的改变来看,似无从下手。如果我们变换一下思路,将上列平衡体系中的 Fe3+、SCN-和 Fe(SCN)3均虚拟为气态物质(虚拟其状态),则向平衡体系中加水,可认为增大了容器的容积,即减小了气体反应物的压强(或浓度),平衡就向气体体积扩大的方向(即上列反应的逆反应方向)移动,这样液体颜色就会变浅。可见 B 项可选而 C 项不可选。
若采用极限思维,对于 B 选项,可作如下设想:加入的水不是很少而是很多,这样上列平衡体系中,Fe3+与 SCN-相互碰撞结合成 Fe(SCN)3分子的机会越稀越少,而 Fe(SCN)3分子电离成 Fe3+和 SCN-的机会则越来越多,无疑是加水的结果,平衡是向逆反应方向移动的,故而溶液颜色变浅。
Fe3++3SCN-
 Fe(SCN)3
Fe(SCN)3等系列反应。可见加入 KCl 晶体,对此平衡无影响;但加入 2 滴 1 mol·L-1的 FeCl3(aq),使溶液中 Fe3+浓度增大,平衡则向正反应方向移动,溶液颜色变深。A、D 项皆不可选。
对于 B、C 选项,因平衡体系中的水量发生了改变,导致溶液中所有溶质的浓度或同等程度地增大,或同等程度地减小;若要判断平衡移动的方向,从浓度的改变来看,似无从下手。如果我们变换一下思路,将上列平衡体系中的 Fe3+、SCN-和 Fe(SCN)3均虚拟为气态物质(虚拟其状态),则向平衡体系中加水,可认为增大了容器的容积,即减小了气体反应物的压强(或浓度),平衡就向气体体积扩大的方向(即上列反应的逆反应方向)移动,这样液体颜色就会变浅。可见 B 项可选而 C 项不可选。
若采用极限思维,对于 B 选项,可作如下设想:加入的水不是很少而是很多,这样上列平衡体系中,Fe3+与 SCN-相互碰撞结合成 Fe(SCN)3分子的机会越稀越少,而 Fe(SCN)3分子电离成 Fe3+和 SCN-的机会则越来越多,无疑是加水的结果,平衡是向逆反应方向移动的,故而溶液颜色变浅。

练习册系列答案
相关题目
 2Fe(SCN)3+3K2SO4达到平衡后,加入少量下列固体物质,该平衡几乎不发生移动的是:
2Fe(SCN)3+3K2SO4达到平衡后,加入少量下列固体物质,该平衡几乎不发生移动的是: X2(g)+Y2(g)达到平衡的标志是( )
X2(g)+Y2(g)达到平衡的标志是( ) 2SO3(g)(正反应为放热反应)
2SO3(g)(正反应为放热反应)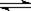 2SO3(g);△H=-196.6kJ/mol
2SO3(g);△H=-196.6kJ/mol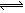 2Z(g),并达平衡,以Y的浓度改变表示的反应速度与时间t的关系如图所示,则Y的平衡浓度表达式正确的是(式中S是对应区域的面积)( )
2Z(g),并达平衡,以Y的浓度改变表示的反应速度与时间t的关系如图所示,则Y的平衡浓度表达式正确的是(式中S是对应区域的面积)( )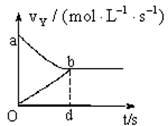
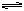 2C
2C CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是
CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是