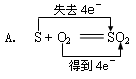
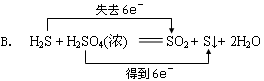
题目内容
已知2.5克KClO3粉未和5.2克研细的碘在一定条件下按下式定量反应:
a KClO3 + bI2 + cHCl = eIClx + fKCl + gH2O,其中x的取值为
a KClO3 + bI2 + cHCl = eIClx + fKCl + gH2O,其中x的取值为
| A.1 | B.3 | C.5 | D.7 |
B
氯酸钾和碘单质的物质的量分别是0.02mol,则氯酸钾在反应中得到0.12mol,所以1mol单质碘即失去6mol电子,则碘在氧化产物中的价态是+3价,即x=3,答案选B。

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
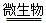 4H++2Fe2++________;
4H++2Fe2++________;