题目内容
下列反应中必须加入氧化剂才能进行的是( )
| A.Cl2→Cl- | B.Zn2+→Zn | C.H2→H2O | D.CuO→CuCl2 |
C
试题分析:A、Cl2→Cl-氯元素化合价由0价降低为-1价,发生还原反应,需加入还原剂才能实现,故A正确;B、Zn→Zn2+锌元素化合价由0价升高为+2价,发生氧化反应,需加入氧化剂才能实现,故B错误;C、H2→H2O氢元素化合价由0价升高为+1价,发生氧化反应,需加入氧化剂才能实现,故C错误;D、CuO→CuCl2铜元素化合价未发生变化,不是氧化还原反应,可通过CuO与盐酸反应实现,故D错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
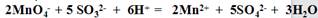
 粒子的空间构型为正四面体型;CO2、C2H2均为直线型分子
粒子的空间构型为正四面体型;CO2、C2H2均为直线型分子 ;NH4Cl的电子式为
;NH4Cl的电子式为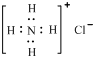
 2Cu+SO2
2Cu+SO2
 Cu + H2O
Cu + H2O 2CO2
2CO2
 2SO3(g )△H=" -Q" kJ·mol-1
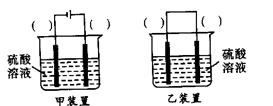
2SO3(g )△H=" -Q" kJ·mol-1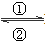 Fe3+的转化时, ①中的Fe2+作________剂,②中的Fe3+作___________剂。
Fe3+的转化时, ①中的Fe2+作________剂,②中的Fe3+作___________剂。 2CO2(g)+N2(g),已知该反应的平衡常数极大(570 K时为1×1059),但反应速率极慢。下列说法正确的是
2CO2(g)+N2(g),已知该反应的平衡常数极大(570 K时为1×1059),但反应速率极慢。下列说法正确的是