题目内容
2.下列叙述:①中国科学家于1965年首次人工合成了具有生物活性的蛋白质--结晶牛胰岛素; ②瑞典化学家贝采利乌斯首次提出了“有机化学”的概念;③德国化学家维勒首次人工合成了有机物--尿素;④德国化学家李比希首创了有机物的定量分法方法和“基团”理论.其中正确的是( )| A. | ① | B. | ①③ | C. | ①②③ | D. | ①②③④ |
分析 ①我国首次人工合成具有生物活性的结晶牛胰岛素;
②贝采利乌斯提出了有机化学的概念;
③1824年,德国化学家维勒首次人工合成尿素;
④根据德国化学家李比希的贡献来分析.
解答 解:①1965年,我国首次人工合成具有生物活性的结晶牛胰岛素,一种具有生物活性的蛋白质,故①正确;
②贝采利乌斯是瑞典化学家,最先提出了有机化学的概念,故②正确;
③1824年,德国化学家维勒首次人工合成尿素,标志着化学肥料的诞生.之后化肥参全世界普遍应用,使粮食产量大幅度增长,故③正确;
④在有机化学发展的进程中,德国化学家李比希的“基团理论”对有机化学的发展起到了巨大的推动作用,故④正确;
故选D.
点评 本题主要考查了化学史,难度不大,平时注意知识的积累.

练习册系列答案
相关题目
13.下列反应既属于氧化还原反应,又属于吸热反应的是( )
| A. | 氢氧化钠与稀盐酸反应 | B. | 锌与稀硫酸反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 灼热的炭与二氧化碳反应 |
10.下列关于营养物质的说法正确的是( )
| A. | 油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物 | |
| B. | 油脂经皂化反应后,可用饱和食盐水使硬脂酸钠析出 | |
| C. | 2mol蔗糖的水解产物是1mol葡萄糖和1mol果糖 | |
| D. | 淀粉溶液和稀硫酸共热后发生水解反应,冷却后加少量银氨溶液,水浴加热后会出现光亮的银镜 |
17.(Ⅰ)观察图A、B、C,回答下列问题:
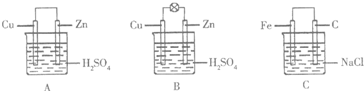
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片没有(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,正极的电极反应式为2H++2e-=H2↑.
(2)如果烧杯中最初装入的是2mol/L 500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线到铜电极),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol/L、c(ZnSO4)=1mol/L.
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,写出正极的电极反应式O2+2H2O+4e-=4OH-.
(Ⅱ)将铜粉末用10%H2O2和3.0mol•L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是温度升高H2O2的分解速率加快,导致H2O2的浓度降低从而使铜的溶解速率慢.

(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片没有(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,正极的电极反应式为2H++2e-=H2↑.
(2)如果烧杯中最初装入的是2mol/L 500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线到铜电极),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol/L、c(ZnSO4)=1mol/L.
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,写出正极的电极反应式O2+2H2O+4e-=4OH-.
(Ⅱ)将铜粉末用10%H2O2和3.0mol•L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
7.下列有关化学用语正确的是( )
| A. | 氯化氢分子的电子式: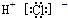 | |
| B. | H2O的结构式:H-O-H | |
| C. | 硫原子的结构示意图: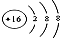 | |
| D. | 原子核内有8个中子的氧原子:${\;}_{8}^{18}$O |
14.表中实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 向苯酚溶液中滴加稀溴水 | 观察白色沉淀三溴苯酚 |
| B | 向待测液中加入碳酸钠溶液 | 鉴别乙酸、乙酸乙酯、乙醇 |
| C | 向3ml5%CuSO4溶液中滴加3-4滴2%氢氧化钠溶液,再向其中加入0.5ml乙醛,加热 | 检验醛基 |
| D | 将溴乙烷与氢氧化钠溶液共热,冷却,继续滴加硝酸银溶液 | 检验溴乙烷中的溴元素 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法正确的是( )
| A. | π键是由两个p轨道“头碰头”重叠形成的 | |
| B. | σ键一定是有s轨道参与形成的 | |
| C. | 甲烷分子中的键全为σ键而乙烯分子中含σ键和π键 | |
| D. | H2分子中含σ键而Cl2分子中还含π键 |
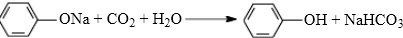 .
.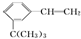 有如下性质:
有如下性质: