题目内容
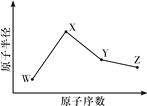
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。
(1)X位于元素周期表中的位置是____________________。
(2)Z的气态氢化物和溴化氢相比,较稳定的是____________(写化学式)。
(3)W与X形成的一种化合物和水反应能生成W的单质,请写出该反应的化学方程式:________________________________________________________________________。
(4)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是________________________________________________________________________。
【答案】 第三周期第ⅠA族 HCl 2Na2O2+2H2O===4NaOH+O2↑ SiCl4+3H2O===H2SiO3↓+4HCl
【解析】W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,可知W的质子数为8,则W是氧元素;X和Ne原子的核外电子数相差1,且原子半径比W大,可知X为11号元素,故X为Na元素;Y的原子半径介于X和W之间,Y的单质是一种常见的半导体材料,所以Y是Si元素;Z的非金属性在同周期元素中最强,原子序数大于Si,故Z为Cl元素,则(1)Na位于元素周期表中的位置是第三周期第ⅠA族。(2)氯元素非金属性强于溴,则氯化氢的稳定性强于溴化氢。(3)W与X形成的一种化合物和水反应能生成W的单质,该反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑。(4)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,强酸是盐酸,弱酸是硅酸,该反应的化学方程式是SiCl4+3H2O=H2SiO3↓+4HCl。