题目内容
【题目】短周期元素a、b、c、d、e在周期表中的相对位置如图所示。已知a元素形成的物质种类最多。
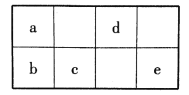
回答下列问题:
(1)在周期表中,b在元素周期表中的位置为______。
(2)b、c、e的气态氢化物热稳定性由强到弱的顺序为_____(用化学式表示)。
(3)在d的氢化物中,既含极性键又含非极性键的分子的电子式为____。
(4)a的单质在过量的d的单质气体中燃烧生成气态产物,转移1mol电子时放出的热量为98.75kJ。写出反应的热化学方程式:_______。
(5)请写出e单质与石灰乳制成漂白粉的化学方程式________。
【答案】第三周期第ⅣA族 HCl>PH3>SiH4 ![]() C(s)+O2(g)=CO2(g)△H=-395kJ/mol 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C(s)+O2(g)=CO2(g)△H=-395kJ/mol 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
【解析】
(1)根据b在元素周期表的位置,推出b为Si元素,所以Si在第三周期第ⅣA族;
(2)根据元素周期表的位置推断,b、c、e分别为Si、P、Cl,氢化物的热稳定性与它的非金属性有关,同一周期依次递增,所以HCl>PH3>SiH4;
(3)在d的氢化物中,既含极性键又含非极性键的分子是过氧化氢;
(4)根据燃烧热的定义进行书写,要注意1mol纯物质;
(5)氯气和氢氧化钙反应生成次氯酸钙、氯化钙和水。
(1)根据周期数和主族数得出;
(2)根据元素周期表的位置推断,b、c、e分别为Si、P、Cl,热稳定性根据非金属性来判断;
(3)在d的氢化物中,既含极性键又含非极性键的分子是过氧化氢,电子式为![]() ;
;
(4)根据燃烧热的定义进行书写,要注意1mol纯物质,C变成CO2失去4个电子,所以方程式为C(s)+O2(g)=CO2(g)△H=-395kJ/mol;
(5)氯气和氢氧化钙反应生成次氯酸钙、氯化钙和水,方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。

【题目】已知部分弱酸的电离平衡常数如下表所示:
弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
电离平衡常数Ka(25℃) | 1.75×10-5 | 2.98×10-8 | Ka1=4.3×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-7 Ka2=1.02×10-7 |
下列离子方程式正确的是
A. 少量的CO2通入NaClO溶液中:CO2+H2O+2C1O-==CO32-+2HClO
B. 少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-==SO32-+2HCO3-
C. 少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-==CaSO3↓+2HClO
D. 相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-==CO2↑+H2O