题目内容
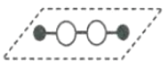
【题目】利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系

回答下列问题:
(1)X的电离方程式为________。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=______。
(3)Y可用于实验室制O2,其焰色试验为紫色,则Y含有的化学键类型为__;Y在400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,生成的两种盐的化学式分别__。
(4)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的__倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示)。
(5)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为__。
【答案】HClO4=H++ClO4- 2:3或![]() 离子键、极性共价键或共价键或极性键 KCl、KClO4 2 2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O
离子键、极性共价键或共价键或极性键 KCl、KClO4 2 2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O
【解析】
(1)X是氯元素的+7价的酸,则X为HClO4,高氯酸为强酸,完全电离,其电离方程式为HClO4=H++ClO4-;
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则有![]() ,故有m:n=2:3;
,故有m:n=2:3;
(3)Y可用于实验室制O2,其焰色试验为紫色,故含有K元素,Y中氯元素的化合价为+5价,则Y为KClO3,含有的化学键类型为离子键、极性共价键或共价键或极性键;KClO3在400℃时分解只生成两种盐,其中一种是无氧酸盐KCl,另一种盐的阴阳离子个数比为1:1,KClO3、KCl中氯元素的化合价分别为+5、-1,根据化合价变化及氧化还原反原理可知,另一种盐中氯元素的化合价应高于+5价,且氯元素的价态一般为奇数价,故为KClO4,即生成的两种盐的化学式分别为KCl、KClO4;
(4)Z是氯元素形成的单质,则为Cl2,NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Cl2的![]() =2倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示);
=2倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示);
(5)Cl2O可用潮湿的Cl2与Na2CO3反应制取,同时生成NaHCO3,反应中Cl2既体现氧化性,又体现还原性,Cl2O中氯为+1价,生成Cl2O时氯气体现还原性,则生成物中还有含氯化合价小于0的,则为Cl-,即有NaCl生成,结合氧化还原反应配平得反应的化学方程式为2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O。

 阅读快车系列答案
阅读快车系列答案