题目内容
15.电子构型中属于原子的基态电子排布的是( )| A. | 1s22s2 | B. | 1s22s23p2 | C. | 1s22s22p63s23d5 | D. | 1s22s22p63s24d1 |
分析 处于最低能量的原子叫做基态原子,基态电子排布遵循能量最低原理、保里不相容原理和洪特规则,以此解答该题.
解答 解:A.基态原子的电子排布式应为1s22s2,符合基态电子排布规律,故A正确;
B.基态原子的电子排布式应为1s22s22p2,发生电子跃迁为1s22s23p2,故B错误;
C.基态原子的电子排布式应为1s22s22p63s23p5,发生电子跃迁为1s22s22p63s23d5,故C错误;
D.基态原子的电子排布式为1s22s22p63s23p1,发生电子跃迁为1s22s22p63s24d1,故D错误.
故选:A.
点评 本题考查核外电子排布,题目难度不大,注意基态电子排布规律与能量跃迁的关系.

练习册系列答案
相关题目
3.如图所示,试管中的物质M可能是( )
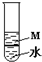

| A. | 四氯化碳 | B. | 乙醇 | C. | 已烷 | D. | 溴苯 |
10.下列说法正确的是( )
| A. | 将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分期得到A12O3、Na2SO3 | |
| B. | 在溶液的稀释过程中,离子浓度有的可能增大,有的可能减小,有的可能不变 | |
| C. | Ksp(BaSO4)=1.08×10-10,Ksp(BaCO3)=8.1×10-9,则沉淀BaSO4不可能转化为BaCO3 | |
| D. | 0.1mo1•L-1CH3COOH溶液在稀释过程中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$将变小 |
7. 如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )
如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )
 如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )
如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )| A. | 该硫酸的浓度为18.4mol•L-1 | |
| B. | 配制200mL 4.6mol•L-1的稀硫酸需该硫酸50mL | |
| C. | 配制100g10%的硫酸需要用到的仪器有胶头滴管、烧杯、玻璃棒、100mL量筒、天平 | |
| D. | 稀释该浓硫酸时可直接把水加入浓硫酸中 |
4.下列分子的空间构型为三角锥形的是( )
| A. | CO2 | B. | H2O | C. | NH3 | D. | H2 |
5.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 11.2 L氧气与臭氧的混合气体中含NA个氧原子 | |
| B. | 60 g SiO2晶体中含有2NA个Si-O键 | |
| C. | 标准状况下,22.4 LSO2的中心原子所含有的孤电子对数为2NA | |
| D. | 常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
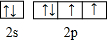 ,该元素的名称是氧;
,该元素的名称是氧;