题目内容
【题目】目前,一种新的制备联氨(N2H4)的方法分为两步。
第一步: NH3和Cl2在液态丙酮![]() 中反应合成异肼
中反应合成异肼![]() ,同时有“白烟”产生;
,同时有“白烟”产生;
第二步:异胼水解生成联氨和丙酮。
巳知:通常条件下,联氨是易吸收水和CO2的液体:碱性条件下,能与AgNO3溶液反应生成Ag和N2。
请回答下列问题:
某小组在实验室应用上述方法制备联氨水合物并测定该水合物的组成,设计实验如下(夹持装置略去)。
I.联氨水合物的制备。
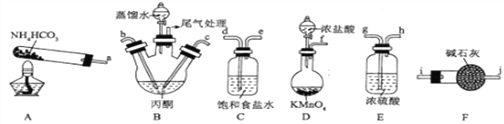
(1)上述装置正确的连接顺序为a―(________)―bc― ( )― ( ) f(填仪器接口字母),盛放丙酮的仪器名称为____________。
(2)用连接好的装置进行实验;
①检验装置的气密性,加入药品;
②排尽装置中的空气;
③向丙酮中缓慢通入NH3和Cl2,进行第一步反应,该反应的化学方程式为____________。 设计实验证明“白烟”的主要成分为NH4Cl:____________;
④完全反应后,再向其中滴加足量蒸馏水,发生第二歩反应。
Ⅱ.测定联氨水水合物的组成。
(3)实验步骤:
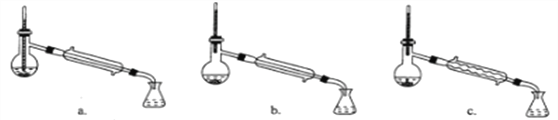
①取装置B中完全反应后的液体,蒸馏,收集联氨水合物。下列蒸馏装置中合理的是________(填选项字母,夹持装置略去),若蒸馏操作开始后,发现蒸馏烧瓶中没有添加沸石,处理方法为_______________。
②取5.0 g联氨水合物,加人适量NaOH溶液,再加人足量AgNO3溶液;充分反应后,过滤、洗涤、干燥、称量,得固体质量为43.2g,则联氨水合物的化学式为_________________。
【答案】 ij、hg、ed 三颈瓶(或三颈圆底烧瓶) 4NH3+Cl2+ 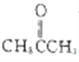 =
=  收集少量白烟,加适量水溶解,将溶液分为两份,一份加入硝酸酸化的AgNO3溶液,有白色沉淀生成;另一份加入NaOH,加热,产生能使湿润的红色石蕊试纸变蓝的气体,则白烟的主要成分为NH4Cl2 b 停止实验,冷却至室温,补加沸石,继续实验 N2H4·H2O
收集少量白烟,加适量水溶解,将溶液分为两份,一份加入硝酸酸化的AgNO3溶液,有白色沉淀生成;另一份加入NaOH,加热,产生能使湿润的红色石蕊试纸变蓝的气体,则白烟的主要成分为NH4Cl2 b 停止实验,冷却至室温,补加沸石,继续实验 N2H4·H2O
【解析】(1)根据反应原理装置连接包括氨气的制备与净化干燥、氯化氢的制备与除杂干燥再一起通入B装置中,根据气流方向装置连接顺序为a―ij―bc―hg―ed―f;
(2)③向丙酮中缓慢通入NH3和C12,进行第一步反应,合成异肼![]() ,同时有“白烟”即NH4Cl产生;根据原子守恒得该反应的化学方程式为4NH3+Cl2+
,同时有“白烟”即NH4Cl产生;根据原子守恒得该反应的化学方程式为4NH3+Cl2+ 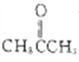 =
=  ;收集少量白烟,加适量水溶解,将溶液分为两份,一份加入硝酸酸化的AgNO3溶液,有白色沉淀生成;另一份加入NaOH,加热,产生能使湿润的红色石蕊试纸变蓝的气体,则白烟的主要成分为NH4Cl;
;收集少量白烟,加适量水溶解,将溶液分为两份,一份加入硝酸酸化的AgNO3溶液,有白色沉淀生成;另一份加入NaOH,加热,产生能使湿润的红色石蕊试纸变蓝的气体,则白烟的主要成分为NH4Cl;
(3)①蒸馏操作时温度计是测蒸气温度的,只能插入到支管口,并利用冷凝管冷却蒸气,选项b装置相对比较合理,若蒸馏操作开始后,发现蒸馏烧瓶中没有添加沸石,停止实验,冷却至室温,补加沸石,继续实验;
② N2H4与足量AgNO3溶液生成43.2gAg和N2,根据电子守恒N2H4的物质的量为![]() ×1÷[0-(-2)×2]=0.1mol,5.0g联氨水合物中水的物质的量为
×1÷[0-(-2)×2]=0.1mol,5.0g联氨水合物中水的物质的量为![]() =0.1mol,N2H4与水的物质的量之比为1:1,则联氨水合物的化学式为 N2H4·H2O。
=0.1mol,N2H4与水的物质的量之比为1:1,则联氨水合物的化学式为 N2H4·H2O。

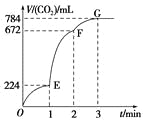
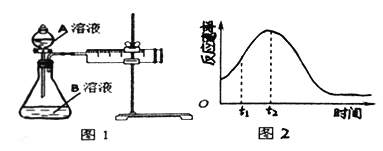
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如表(KMnO4溶液用稀硫酸酸化),实验装置如图1:
实验序号 | A溶液 | B溶液 |
① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.0lmol·L-1KMnO4溶液 |
② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.01mol·L-1KMnO4溶液 |
(1)该反应的化学方程式为__________。
(2)该实验探究的是__________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积
大小关系是__________ < __________ (填实验序号)。
(3)若实验①在2min末收集了 2.24mLCO2 (标准状况下),则在2min末,c(MnO4-) =__________ mol·L-1。(假设混合溶液体积为50mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定__________来比较化学反应速率。(一条即可)
(5)小组同学发现反应速率随时间的变化如图2所示,其中t1t2时间内速率变快的主要原因可能是:
①__________ ; ②__________ 。