题目内容
某实验小组利用饱和食盐水、导线、直流电源(用 “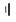 ”或“
”或“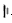 ”表示)、烧杯、灵敏电流计(用“
”表示)、烧杯、灵敏电流计(用“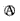 ”表示)和两个电极棒(分别是M、N) 进行电化学实验探究。
”表示)和两个电极棒(分别是M、N) 进行电化学实验探究。
甲同学安装好仪器,接好直流电源通电几分钟,发现M处溶液逐渐变浅绿色,过一段时间,溶液变得浑浊且逐渐出现红棕色。
乙同学所用的仪器和甲同学的看上去相同,但接好直流电源通电几秒钟,却闻到一股刺鼻的气味,马上停止通电。
丙同学安装好仪器,线路闭合几秒钟后,却没有发现明显现象,他又很快接入灵敏电流计,发现电流计的指针发生了偏转。 请根据上述同学的实验现象回答以下问题:
(1)M电极棒材料是(写化学式)___________,N电极棒材料是(写化学式)____________。
(2)在下列虚框内完成对应三个同学的装置图:
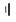 ”或“
”或“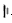 ”表示)、烧杯、灵敏电流计(用“
”表示)、烧杯、灵敏电流计(用“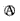 ”表示)和两个电极棒(分别是M、N) 进行电化学实验探究。
”表示)和两个电极棒(分别是M、N) 进行电化学实验探究。 甲同学安装好仪器,接好直流电源通电几分钟,发现M处溶液逐渐变浅绿色,过一段时间,溶液变得浑浊且逐渐出现红棕色。
乙同学所用的仪器和甲同学的看上去相同,但接好直流电源通电几秒钟,却闻到一股刺鼻的气味,马上停止通电。
丙同学安装好仪器,线路闭合几秒钟后,却没有发现明显现象,他又很快接入灵敏电流计,发现电流计的指针发生了偏转。 请根据上述同学的实验现象回答以下问题:
(1)M电极棒材料是(写化学式)___________,N电极棒材料是(写化学式)____________。
(2)在下列虚框内完成对应三个同学的装置图:
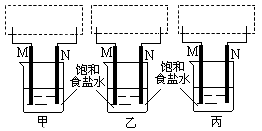
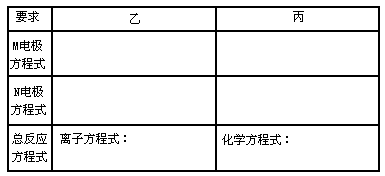
(3)按下表要求写出三个同学实验过程中涉及的反应方程式:
(4)用化学方程式解释甲同学实验时观察到M处溶液出现浑浊后转为红棕色现象的原因:________。
(5)丙同学为了保护M电极不被腐蚀,他可以将N电极棒更换为(写化学式) __________。为验证该防护方法有效,他又做下列对比实验:接通电路2分钟后,分别在M电极区滴入2滴黄色K3Fe(CN)6]溶液,发现没有更换N电极棒的烧杯中的现象是__________,发生反应的离子方程式是____________ ,他还可选用的检验试剂是____________。
(5)丙同学为了保护M电极不被腐蚀,他可以将N电极棒更换为(写化学式) __________。为验证该防护方法有效,他又做下列对比实验:接通电路2分钟后,分别在M电极区滴入2滴黄色K3Fe(CN)6]溶液,发现没有更换N电极棒的烧杯中的现象是__________,发生反应的离子方程式是____________ ,他还可选用的检验试剂是____________。
(1) Fe ;C(或Pt等惰性电极)
(2)
(3)2H++2e-=H2↑ ;Fe-2e-=Fe2+ ;2Cl--2e-=Cl2↑ ;O2+2H2O+4e-=4OH- ;2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
2Fe+O2+2H2O=2Fe(OH)2
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(5)Zn(合理即可);溶液中产生蓝色沉淀 ;3Fe2++2[Fe( CN)6 ]3-=Fe3[Fe(CN)6]2↓ ;酸性KMnO4溶液或KSCN溶液和氯水
(2)

(3)2H++2e-=H2↑ ;Fe-2e-=Fe2+ ;2Cl--2e-=Cl2↑ ;O2+2H2O+4e-=4OH- ;2Cl-+2H2O
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH- 2Fe+O2+2H2O=2Fe(OH)2
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(5)Zn(合理即可);溶液中产生蓝色沉淀 ;3Fe2++2[Fe( CN)6 ]3-=Fe3[Fe(CN)6]2↓ ;酸性KMnO4溶液或KSCN溶液和氯水

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法。
(1)写出硫铁矿与氧气反应的化学方程式:
工业上,该反应在 (填设备名称)中进行。
(2)某含有SiO2的硫铁矿试样1克,在氧气中充分灼烧后残余固体为0.76g,则该硫铁矿式样的纯度为 %
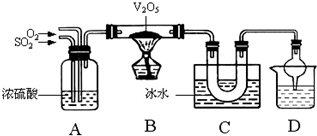
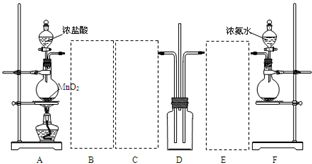
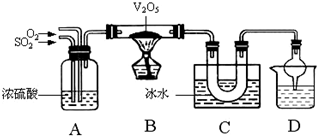
已知SO3熔点16.83℃、沸点44.8℃。某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体。装置如下图所示
 |
(3)写出B中催化剂V2O5表面所发生的反应的化学方程式:
(4)学生实验时发现在C装置U形管的右边有白雾生成。改进的办法是 。
(5)装置D的作用是吸收尾气,其中干燥管的作用是 。装置D
中所装液体试剂可能为( )
A.饱和食盐水 B.酒精 C.BaCl2溶液 D.NaOH溶液
 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.
我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.