题目内容
10.如图:1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g•cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用如图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).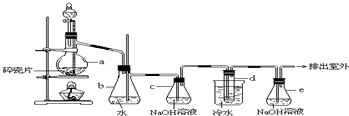
填写下列空白:
(1)浓硫酸的作用是催化剂、脱水剂、吸水剂
(2)写出本题中制备1,2-二溴乙烷的两个化学反应方程式CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O、CH2=CH2+Br2→CH2BrCH2Br,并指出反应的类型消去反应、加成反应;
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象b中水面会下降,玻璃管中的水面会上升,甚至溢出.
(4)容器c中NaOH溶液的作用是:除去乙烯中带出的酸性气体(或除去CO2、SO2).
分析 制备1,2-二溴乙烷,由实验装置可知,分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,加热时发生CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,浓硫酸在该反应中作催化剂、脱水剂、吸水性,b可防止倒吸,且可吸收乙醇,c中NaOH溶液可除去乙烯中的酸性物质,d中发生CH2=CH2+Br2→CH2BrCH2Br,由信息可知,冷水冷却后试管中无色液体为1,2-二溴乙烷,e可吸收尾气中的溴,以此来解答.
解答 解:制备1,2-二溴乙烷,由实验装置可知,分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,加热时发生CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,浓硫酸在该反应中作催化剂、脱水剂、吸水性,b可防止倒吸,且可吸收乙醇,c中NaOH溶液可除去乙烯中的酸性物质,d中发生CH2=CH2+Br2→CH2BrCH2Br,由信息可知,冷水冷却后试管中无色液体为1,2-二溴乙烷,e可吸收尾气中的溴,
(1)由上述分析可知,浓硫酸的作用是催化剂、脱水剂、吸水剂,故答案为:催化剂、脱水剂、吸水剂;
(2)由上述分析可知,涉及的制备反应分别为CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O、CH2=CH2+Br2→CH2BrCH2Br,分别属于消去反应、加成反应,
故答案为:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O、CH2=CH2+Br2→CH2BrCH2Br;消去反应、加成反应;
(3)试管d发生堵塞时,b中压强不断增大,会导致b中水面下降,玻璃管中的水柱上升,甚至溢出,
故答案为:b中水面会下降,玻璃管中的水面会上升,甚至溢出;
(4)浓硫酸使乙醇脱水生成C,与浓硫酸反应生成二氧化碳、二氧化硫等,c中氢氧化钠可以吸收制取乙烯中产生的杂质气体二氧化碳和二氧化硫发生反应,防止造成污染,
故答案为:除去乙烯中带出的酸性气体(或除去CO2、SO2).
点评 本题考查制备实验方案的设计,为高频考点,把握有机物的结构与性质、乙烯的制备实验、乙烯的化学性质及实验装置的作用为解答的关键,侧重分析与实验能力的综合考查,题目难度中等.

| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 2min末浓度/mol•L-1 | 0.08 | a | b |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 平衡时,X的转化率为20% | |
| B. | t℃时,该反应的平衡常数为40 | |
| C. | 前2 min内,用Y的变化量表示的平均反应速率v(Y)=0.03 mol•L-1•min-1 | |
| D. | 增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动 |
(1)工业上可用CO2和H2反应合成甲醇,已知25℃、101kPa下:
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H2=-242kJ•mol-1
CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O△H2=-676kJ•mol-1
①写出CO2与H2反应生成CH3OH(g)与H2O(g)的热化学方程式CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-50 kJ/mol.
②下列表示合成甲醇反应的能量变化示意图中正确的是a(填字母).
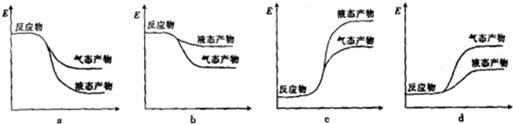
③合成甲醇所需的H2可由下列反应制取:H2O(g)+CO(g)?H2(g)+CO2(g),某温度下该反应的平衡常数K=1,若起始时c(CO)=1mol•L-1,c(H2O)=2mol•l-1,则达到平衡时H2O的转化率为33.3%.
(2)CO和H2反应也能合成甲醇:CO(g)+2H2?CH3OH(g)△H=-90.1kJ•mol-1,在250℃下,将一定量的CO和H2投入10L的恒容密闭容器中,各物质的浓度(mol•L-1)变化如下表所示(前6min没有改变条件):
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
②若6~8min时只改变了一个条件,则改变的条件是加入1mol氢气,第8min时,该反应是否达到平衡状态?不是(填“是”或“不是”)
③该合成反应的温度一般控制在240~270℃,选择此温度的原因是:
Ⅰ.此温度下的催化剂活性高;
Ⅱ.温度低,反应速率慢,单位时间内的产量低,而正反应为放热反应,温度过高,转化率降低.
(3)甲醇在催化剂条件下可以直接氧化成甲酸,在常温下,20.00mL0.1000mol•L-1NaOH溶液与等体积、等浓度甲酸溶液混合后所得溶液的pH>(填“<”“>”或“=”)7,原因是HCOO-+H2O?+HCOOH+OH-(用离子方程式表示).
| A. | 电能是二级能源 | B. | 水力是二级能源 | ||
| C. | 天然气是二级能源 | D. | 焦炉气是一级能源 |
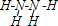 ,分子中氮原子轨道的杂化类型是sp3.
,分子中氮原子轨道的杂化类型是sp3.
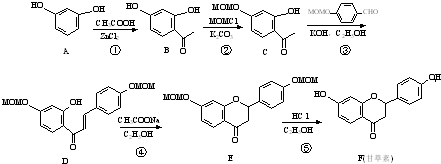
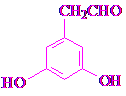 (任写一种).
(任写一种).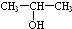 和HCHO为原料制备
和HCHO为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: