题目内容
在一定条件下,CO(g)和H2(g)发生反应:CO(g) + 2H2(g) 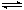 CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表:
CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表:

下列说法中正确的是
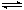 CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表:
CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表:
下列说法中正确的是
| A.热化学方程式中a>0 |
| B.T1℃下,在第一小时内用H2表示的化学反应速率为0.4mol/(L.h) |
| C.T1℃下,该反应的化学平衡常数为25 |
| D.T2℃下,ɑ1=ɑ2﹥80% |
C
试题分析:A、分析题给数据知,第一小时内T2℃时反应速率快,温度T1<T2,结合转化率分析,该反应为放热反应,热化学方程式中a<0,错误;B、根据题给数据分析,T1℃下,在第一小时内CO的物质的量浓度浓度变化为0.4mol/L,结合反应方程式知,H2的浓度变化为0.8mol/L,用H2表示的化学反应速率为0.8mol/(L.h),错误;C、根据题给数据分析,T1℃下,该反应达平衡时各物质的平衡浓度为:CO0.2mol/L,H20.4mol/L,CH3OH0.8mol/L,代入平衡常数表达式计算得化学平衡常数为25,正确;D、分析题给数据知,第一小时内T2℃时反应速率快,先达到平衡,温度T1<T2,结合转化率分析,该反应为放热反应,升温平衡向吸热反应方向移动,T2℃下,ɑ1=ɑ2<80%,错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

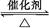 2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为( )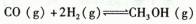


 2NO2(g) ΔH>0。隔一定时间对该容器内的物质进行分析,得到如下数据:
2NO2(g) ΔH>0。隔一定时间对该容器内的物质进行分析,得到如下数据:
 I3-(aq),其平衡常数表达式为
I3-(aq),其平衡常数表达式为