题目内容
【题目】已知:CxHy+H2O→CO+CO2+H2(未配平),工业上用甲烷、乙烷的混合气体利用上述反应生成氢气,反应后气体经干燥组成如下表所示,计算原混合气体中甲烷与乙烷的物质的量之比____________。
组分 | CO | CO2 | H2 |
体积分数 | 20% | 5% | 75% |
【答案】3:1
【解析】
设反应后气体总物质的量为amol,甲烷的物质的量为xmol、乙烷的物质的量为ymol,
则含有CO物质的量而为0.2amol,二氧化碳为0.05amol,氢气为0.75amol,
根据碳元素守恒可得:①x+2y=0.2a+0.05a=0.25a,根据氧元素守恒可知,参加反应的水的物质的量为:0.2a+0.05a×2=0.3a,根据H元素守恒,水分子中H生成氢气的物质的量为0.3a,则甲烷和乙烷分子中含有氢元素生成的氢气的物质的量为:0.75a﹣0.3a=0.45a,即:②![]() (4x+6y)=0.45a,
(4x+6y)=0.45a,
联立①②解得:x=0.15a、y=0.05a,
所以原混合气体中甲烷与乙烷的物质的量之比为:0.15a:0.05a=3:1。

 阅读快车系列答案
阅读快车系列答案【题目】某研究小组将纯净的SO2气体缓缓的通入到盛有25mL0.1mol· L-1的Ba(NO3)2溶液中,得到BaSO4沉淀。为探究该反应中的氧化剂,该小组提出了如下假设:
假设Ⅰ:溶液中的NO3-;
假设Ⅱ:________________。
(1)该小组设计了以下实验验证了假设Ⅰ成立(为排除假设Ⅱ对假设Ⅰ的干扰,在配制下列实验所用溶液时,应___________________),请填写下表。
实验步骤 | 实验现象 | 结论 | |
实验① | 向盛有25mL0.1mol·L-1BaCl2溶液的烧杯中缓慢通入纯净的SO2气体 | ______ | 假设Ⅰ成立 |
实验② | 向盛有25mL0.1mol· L-1Ba(NO3)2溶液的烧杯中缓慢通入纯净的SO2气体 | ______ | |
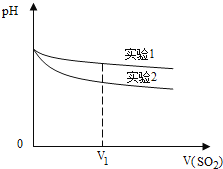
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图。V1时,实验②中溶液pH小于实验①的原因是(用离子方程式表示):________。
(3)验证假设Ⅱ。某同学设计了以下方案,请完成下列表格(可以不填满)。
实验步骤 | 实验现象 | 实验目的 | ||
实验③ | 同实验①步骤 | 同实验①的相关现象 | ______ | |
实验④ | ______ | ______ | ______ | |
(4)查资料知:H2SO3是二元酸(Kl=1.54×10-2,K2=1.02×10-7),请设计实验方案验证H2SO3是二元酸______(试剂及仪器自选)。