题目内容
20.化学与环境保护、工业生产、生活等密切相关.下列说法不正确的是( )| A. | 海水中含有丰富的资源,不经化学反应可从海水中提取溴、镁、氯化钠等物质 | |
| B. | 大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染,使用清洁能源是防止酸雨发生的重要措施之一 | |
| C. | 合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 | |
| D. | 晶体硅可用于光伏发电、制造芯片 |
分析 A.溴、镁在海水中以离子形式存在;
B.硫的氧化物和氮的氧化物能形成酸雨;
C.合理开发利用可燃冰有助于缓解能源紧缺;
D.硅是半导体材料,常用于光伏发电、制造计算机芯片.
解答 解:A.、镁在海水中以离子形式存在,需经化学反应才能提取,故A错误;
B.硫的氧化物和氮的氧化物能形成酸雨,实施矿物燃料“脱硫、脱硝技术”,减少污染物的产生,故B正确;
C.可燃冰为我国在新世纪使用高效新能源开辟了广阔的前景,合理开发利用可燃冰有助于缓解能源紧缺,故C正确;
D.硅具有金属和非金属的性质,是良好的半导体材料,在制作计算机芯片、太阳能电池的主要材料,故D正确.
故选A.
点评 本题考查常见的生活污染及治理方法、材料、化学变化等知识,题目难度中等,侧重于化学与生活、环境的考查,有利于培养学生的良好科学素养.

练习册系列答案
相关题目
11.若NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,6.72LNO2与水充分反应转移电子数为0.1NA | |
| B. | 18gD2O中含有的质子数目为10NA | |
| C. | 常温常压下,1mol氦气中含有的核外电子数为2NA | |
| D. | ag某气体含分子数为b,cg该气体在标况下的体积为$\frac{22.4ab}{c{N}_{A}}$L |
8.化学与社会、生产、生活紧切相关,下列说法正确的是( )
①光导纤维具有很强的导电能力,所以大量用于制造通信光缆
②食盐可作为调味品和防腐剂
③明矾常用作净水剂,是因为它具有消毒杀菌的作用
④SiCl4在战争中常用作烟雾弹,是因为它水解时生成白色烟雾
⑤氨常用作制冷剂,是因为其沸点较低,很容易液化
⑥将过量CO2气体通入C6H5ONa溶液中可生成C6H5OH和碳酸钠.
①光导纤维具有很强的导电能力,所以大量用于制造通信光缆
②食盐可作为调味品和防腐剂
③明矾常用作净水剂,是因为它具有消毒杀菌的作用
④SiCl4在战争中常用作烟雾弹,是因为它水解时生成白色烟雾
⑤氨常用作制冷剂,是因为其沸点较低,很容易液化
⑥将过量CO2气体通入C6H5ONa溶液中可生成C6H5OH和碳酸钠.
| A. | ①②④⑤ | B. | ②④ | C. | ②④⑤ | D. | ②③④⑥ |
15.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,2.24 L CCl4中含有的分子数为0.1NA | |
| B. | 1L 0.1 mol•L-1 NaHCO3溶液中含有0.1NA个HCO3- | |
| C. | 0.1 mo1铁粉在0.1 mol氯气中充分燃烧,失去的电子数目为0.3NA | |
| D. | 1 mol苯含有6 NA个C-H键 |
5. 向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )
向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )
 向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )
向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )| A. | 4mol/L | B. | 3mol/L | C. | 2mol/L | D. | 1mol/L |
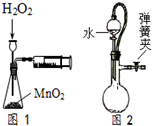
12.下列有关实验原理或实验操作正确的是( )

| A. | 将氯化铁固体溶于稀盐酸配制FeCl3溶液 | |
| B. | 称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol•L-1的NaOH溶液 | |
| C. | 利用图1装置定量测定H2O2的分解速率 | |
| D. | 如图2所示,关闭弹簧夹检查装置的气密性 |
9.了解一些安全生活、生产常识,有助于自身安全及事故救助.下列有关安全处理不合理的是( )
| A. | 木材厂、纺织厂、面粉厂都必须严禁烟火 | |
| B. | 炒菜时锅中的油着火时可立即盖上锅盖 | |
| C. | 运输液氯的罐车泄漏时应逆风往高处跑 | |
| D. | 化学品仓库保存的金属钠着火时可用水灭 |
 为将CO和NO转化为无毒物质,某同学设计了如图装置.
为将CO和NO转化为无毒物质,某同学设计了如图装置.