题目内容
工业上用FeCl3溶液腐蚀印刷线路板,现有一块重250g的印刷线路板投入到500mL 2mol/L FeCl3溶液,一段时间后,取出干燥后称重218g,假设溶液体积不变,则下列说法正确的是( )
| A、在反应后的溶液中滴加KSCN溶液,溶液呈红色 | B、反应后溶液中c(Cl-)=6mol/L | C、反应后溶液中加入铁屑不溶解 | D、反应后溶液中c(Cu2+):c(Fe2+)=1:1 |
分析:发生2FeCl3+Cu═2FeCl2+CuCl2,则减少质量为Cu,其质量为250g-218g=32g,n(Cu)=
=0.5mol,由反应可知,消耗氯化铁为1mol,而n(FeCl3)
=0.5L×2mol/L=1mol,即二者恰好完全反应,以此来解答.
| 32g |
| 64g/mol |
=0.5L×2mol/L=1mol,即二者恰好完全反应,以此来解答.
解答:解:发生2FeCl3+Cu═2FeCl2+CuCl2,则减少质量为Cu,其质量为250g-218g=32g,n(Cu)=
=0.5mol,由反应可知,消耗氯化铁为1mol,而n(FeCl3)
=0.5L×2mol/L=1mol,即二者恰好完全反应,
A.由上述分析可知,铁离子完全反应,则在反应后的溶液中滴加KSCN溶液,溶液不变红色,故A错误;
B.2mol/L FeCl3溶液,氯离子不反应,则c(Cl-)=2mol/L×3=6mol/L,故B正确;
C.反应后溶液中加入铁屑,与氯化铜反应生成Cu,则Fe溶解,故C错误;
D.由反应可知,反应后溶液中c(Cu2+):c(Fe2+)=1:2,故D错误;
故选B.
| 32g |
| 64g/mol |
=0.5L×2mol/L=1mol,即二者恰好完全反应,
A.由上述分析可知,铁离子完全反应,则在反应后的溶液中滴加KSCN溶液,溶液不变红色,故A错误;
B.2mol/L FeCl3溶液,氯离子不反应,则c(Cl-)=2mol/L×3=6mol/L,故B正确;
C.反应后溶液中加入铁屑,与氯化铜反应生成Cu,则Fe溶解,故C错误;
D.由反应可知,反应后溶液中c(Cu2+):c(Fe2+)=1:2,故D错误;
故选B.
点评:本题考查离子反应的计算,为高频考点,把握发生的氧化还原反应及量的关系为解答的关键,侧重分析能力及计算能力的考查,题目难度不大,注意铁离子的检验方法.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
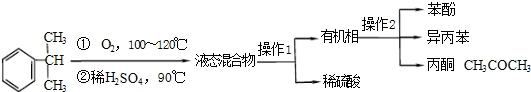
工业上用异丙苯氧化法合成苯酚,其生产流程如下图:
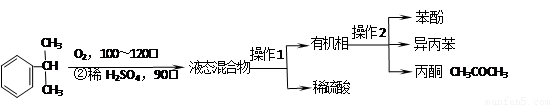
有关物质的性质如下表:
|
物质 |
沸点 |
溶解性 |
主要化学性质 |
|
异丙苯 |
152.4℃ |
不溶于水,易溶于酒精。 |
可被强氧化剂氧化 |
|
苯酚 |
181.8℃ |
微溶于冷水,易溶于热水和酒精等有机溶剂。 |
易被氧化 |
|
丙酮 |
56.2℃ |
易溶于水和有机溶剂 |
不易被氧化 |
(1)检验有机相中是否含有水的方法是 ;
(2)“操作2”的名称是 ;
(3)丙酮中常含有苯酚和异丙苯中的一种或者两种有机物杂质,某同学做了如下检验。
|
检验项目 |
实验方案 |
|
检验丙酮中一定存在有机杂质的方法是 |
A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
|
检验丙酮中一定含有苯酚的方案是: |
取少许待测液置于试管中,滴加1~2滴FeCl3溶液。预期的实验现象和结论是 。 |
(4)某同学对该厂废水进行定量分析。取20.00mL废水于锥形瓶中,水浴加热,用0.1000mol·L-1酸性KMnO4溶液滴定(假定只有苯酚与KMnO4反应)。达到滴定终点时,消耗KMnO4溶液的体积为10.00mL。有关反应方程式为:
5  +
28KMnO4 + 42H2SO4
+
28KMnO4 + 42H2SO4 28MnSO4
+ 14K2SO4 + 30CO2↑+ 57H2O
28MnSO4
+ 14K2SO4 + 30CO2↑+ 57H2O
①滴定终点的现象为 。
②该废水中苯酚的含量为 mg·mL-1。(保留二位有效数字)。