题目内容
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物.试回答下列问题: 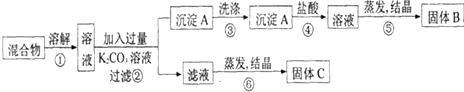
(1)B物质的化学式为 .
(2)该方案的明显失误是因某一步设计不当而使分离产物不纯,该步骤是(填序号)如何改进 .
(3)写出K2CO3的电离方程式 .
(4)写出 ②④两步中对应的离子方程式:
②
④ .
【答案】
(1)BaCl2
(2)⑥;应先在⑥步操作前的滤液中加足量盐酸后,蒸发结晶
(3)K2CO3═2K++CO32﹣
(4)Ba2++CO32﹣═BaCO3↓;BaCO3+2H+═Ba2++CO2↑+H2O
【解析】解:分离KCl和BaCl2两种固体混合物,可先溶于水,然后加入过量K2CO3使BaCl2转化为A碳酸钡沉淀,过滤后沉淀加入盐酸可生成BaCl2溶液,经⑤蒸发、结晶后可得B固体BaCl2 , 操作②所得滤液为KCl和K2CO3的混合物,应加入过量盐酸可得KCl,固体C为KCl;(1)氯化钾和氯化钡溶液中加入碳酸钾溶液可以生成碳酸钡沉淀,则沉淀A为BaCO3;过滤后碳酸钡沉淀中加入盐酸可生成BaCl2溶液,经⑤蒸发、结晶后可得B固体BaCl2 , 所以答案是:BaCl2;(2)蒸发结晶前应加入适量稀盐酸,将过量的碳酸钾转化成氯化钾,否则晶体不纯,所以答案是:⑥;应先在⑥步操作前的滤液中加足量盐酸后,蒸发结晶;(3)K2CO3为强电解质,完全电离,电离方程式为K2CO3═2K++CO32﹣ , 所以答案是:K2CO3═2K++CO32﹣;(4)②加入碳酸钾生成碳酸钡沉淀,反应的离子方程式为Ba2++CO32﹣═BaCO3↓,④为碳酸钡和盐酸的反应,离子方程式为BaCO3+2H+═Ba2++CO2↑+H2O,
所以答案是:Ba2++CO32﹣═BaCO3↓;BaCO3+2H+═Ba2++CO2↑+H2O.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案