��Ŀ����
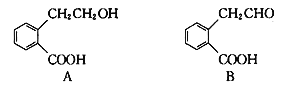
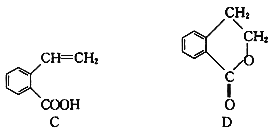
����Ŀ���������ӷ���ʽ��д����ȷ����
A��AlCl3��Һ���ռ���Һ��Ӧ����n(OH)��n(Al3+)=7��2ʱ��2Al3++7OH![]() Al(OH)3��+
Al(OH)3��+![]() +2H2O
+2H2O
B����Na2CO3��Һ��ͨ�������CO2��![]() +CO2+H2O
+CO2+H2O![]() 2
2![]()
C��CuCl2��Һ��NaHS��Һ��Ӧ����n(CuCl2)��n(NaHS)=1��2ʱ��Cu2++2HS![]() CuS��+H2S��
CuS��+H2S��
D��Fe��ϡ���ᷴӦ����n(Fe)��n(HNO3)=1��2ʱ��3Fe+2![]() +8H+
+8H+![]() 3Fe2++2NO��+4H2O
3Fe2++2NO��+4H2O
���𰸡�B
�����������⿼�����ӷ�Ӧ����ʽ����д��A��AlCl3��Һ���ռ���Һ��Ӧ������1��3��Ӧ����������������������1��4��Ӧ����ƫ�����ƣ���n(OH)��n(Al3+)=7��2ʱ����Ӧ���ɲ���Ϊ��������������ƫ�����ƣ���ƽ�õ����ӷ���ʽΪ��2Al3++7OH![]() Al(OH)3��+
Al(OH)3��+![]() +2H2O����A��ȷ��B����Na2CO3��Һ��ͨ�������CO2�����ɵ�̼�����Ʋ���ȫ������ˮ����һ���ֻ�������B����C��CuCl2��Һ��NaHS��Һ��Ӧ����n(CuCl2)��n(NaHS)=1��2ʱ��Cu2++2HS
+2H2O����A��ȷ��B����Na2CO3��Һ��ͨ�������CO2�����ɵ�̼�����Ʋ���ȫ������ˮ����һ���ֻ�������B����C��CuCl2��Һ��NaHS��Һ��Ӧ����n(CuCl2)��n(NaHS)=1��2ʱ��Cu2++2HS![]() CuS��+H2S�������Ϸ�Ӧԭ�����غ㣬C��ȷ��D�� Fe��ϡ���ᷴӦ����n(Fe) ��n(HNO3)=1��2ʱ�������������ӷ���ʽ��3Fe+2
CuS��+H2S�������Ϸ�Ӧԭ�����غ㣬C��ȷ��D�� Fe��ϡ���ᷴӦ����n(Fe) ��n(HNO3)=1��2ʱ�������������ӷ���ʽ��3Fe+2![]() +8H+
+8H+![]() 3Fe2++2NO��+4H2O��D��ȷ����ѡB��
3Fe2++2NO��+4H2O��D��ȷ����ѡB��

 ��ҵ����ϵ�д�
��ҵ����ϵ�д�����Ŀ����һ���¶�����������X������Y��0.16 mol����10 L�����ܱ���������������Ӧ��X(g)+Y(g) ![]() 2Z(g)����H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±�������˵����ȷ����
2Z(g)����H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±�������˵����ȷ����
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. ��Ӧǰ2 min��ƽ������v(Z)=2.0��10-3 mol��L-1��min-1
B. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ��v(��)>v(��)
C. ���������������䣬��ʼʱ�������г���0.32 mol����X��0.32 mol ����Y������ƽ��ʱ��n(Z)=0.24 mol
D. ���¶��´˷�Ӧ��ƽ�ⳣ����K=1.44