题目内容
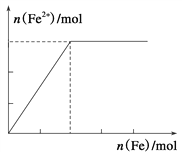
【题目】向某HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如下图所示,则原稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比为( )
A. 4∶1 B. 3∶1 C. 2∶1 D. 1∶1
【答案】A
【解析】根据题干信息可知混合溶液中加入铁粉发生的反应为:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,2Fe(NO3)3+Fe=3Fe(NO3)2,由图象可知,加入2molFe粉时,铁离子完全反应生成Fe2+的物质的量为3mol,设混合溶液中有x mol HNO3,y mol Fe(NO3)3,则: ![]() 、
、![]() ,解得y=1、x=4,故原稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比4:1,答案选A。
,解得y=1、x=4,故原稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比4:1,答案选A。

练习册系列答案
相关题目