题目内容
【题目】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
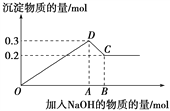
(1)写出代表各线段发生的反应的离子方程式:
OD段________________________________________________,
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为________。
(3)图中C点表示当加入______mol NaOH时,Al3+已经转化为_____,Mg2+已经转化为______。
(4)图中线段OA∶AB=________。
【答案】 Mg2++2OH-===Mg(OH)2↓、Al3++3OH-===Al(OH3)↓ Al(OH)3+OH-==AlO2-+2H2O 2∶1 0.8 AlO![]() Mg(OH)2 7∶1
Mg(OH)2 7∶1
【解析】试题分析:(1)OD段镁离子和铝离子全部转化为沉淀,其离子方程式为Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓;DC段NaOH过量时氢氧化铝溶解,其离子方程式为:Al(OH)3+OH-═AlO2-+2H2O。
(2)由图象可知,0~A发生Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,A~B发生Al(OH)3+OH-═AlO2-+2H2O,C点对应的沉淀为Mg(OH)2,D点对应的沉淀为Mg(OH)2和Al(OH)3,则Mg(OH)2的物质的量为0.2mol,Al(OH)3的物质的量为0.3mol-0.2mol=0.1mol,由Mg(OH)2~Mg2+、Al(OH)3~Al3+,溶液的体积相同,浓度之比等于物质的量之比,所以原溶液中Mg2+、Al3+物质的量浓度之比为0.2mol:0.1mol=2:1。
(3)由Mg2++ 2OH-═Mg(OH)2↓
0.2mol 0.4mol
Al3++ 3OH- ═Al(OH)3↓
0.1mol 0.3mol
Al(OH)3+OH-═AlO2-+2H2O
0.1mol 0.1mol
则C点NaOH的物质的量为0.4mol+0.3mol+0.1mol=0.8mol,此时铝离子完全转化为AlO2-,镁离子完全转化为Mg(OH)2沉淀。
(4)0~A发生Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,A~B发生Al(OH)3+OH-═AlO2-+2H2O,则线段OA对应的NaOH的物质的量为0.4mol+0.3mol=0.7mol,线段AB对应的NaOH的物质的量为0.1mol,所以线段OA:AB=0.7mol:0.1mol=7:1。

【题目】二氧化硫是硫的重要化合物,在生产、生活中有广泛应用.二氧化硫有毒,并且是形成酸雨的主要气体.无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要.完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫. 
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是(填写字母).
(2)若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,至少需要称取亚硫酸钠g(保留一位小数);如果已有40%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠g (保留一位小数).
(3)实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通.石灰﹣石膏法和碱法是常用的烟气脱硫法.
石灰﹣石膏法的吸收反应为SO2+Ca(OH)2→CaSO3↓+H2O.吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O→2CaSO42H2O.其流程如图1,碱法的吸收反应为SO2+2NaOH→Na2SO3+H2O.碱法的特点是氢氧化钠碱性强、吸收快、效率高.其流程如图2:
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰﹣石膏法和碱法吸收二氧化硫的化学原理相同之处是 . 和碱法相比,石灰﹣石膏法的优点是 , 缺点是 .
(4)在石灰﹣石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示).
【题目】工业上通常采用N2(g)和H2(g)崔华成NH3(g):N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1
(1)在一定温度下,若将10amolN2和30amolH2放入2L的密闭容器中,充分反应后测得平衡时N2的转化率为60%,则该反应的平衡常数为(用含a的代数式表示).若此时再向该容器中投入10amolN2、20amolH2和20amolNH3 , 判断平衡移动的方向是(填“正向移动”“逆向移动”或“不移动”).
(2)若反应起始时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L.则NH3达到平衡时浓度的范围为;若平衡时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L,则NH3起始时浓度的范围为 .
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
容器 | 甲 | 乙 | 丙 | |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 | |
平衡时数据 | 反应能量变化的绝对值(kJ) | Q1 | Q2 | Q3 |
反应物转化率 | a1 | a2 | a3 | |
体系压强(Pa) | p1 | P2 | P3 | |
则Q1+Q2=kJ;a1+a2l(填“<”“>”或“=”下同):2p2p3
(4)如图:A是恒容的密闭容器,B是一个体积可变的充气气囊.保持恒温,关闭K2 , 将1molN2和3molH2通过K3充入B中,将2molN2和6molH2通过K1充入A中;起始时A、B的体积相同均为1L,达到平衡时,V(B)=0.9L;然后打开K2 , 一段时间又达到平衡时,B的体积为L(连通管中气体体积不计). 
【题目】实验室制取乙烯的传统做法是采用浓硫酸做催化剂,由于浓硫酸具有具有脱水性和强氧性,生成乙烯同时产生CO2和SO2气体会影响乙烯的性质实验.某同学查阅相关资料后发现,可用脱水性更强的P2O5代替浓硫酸浓硫酸作为该实验的催化剂.为验证这一说法,该同学利用以下装置进行实验探究,观察并记录现象如下: 
实验一 | 实验二 | |
实验药品 | 4g P2O5、8mL无水乙醇 | |
实验条件 | 酒精灯加热 | 水浴加热 |
实验现象 | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇,立即产生白雾,当用酒精灯加热后,有气泡产生,并逐渐沸腾,生成粘稠状液体,集气瓶C中有无色液体产生. | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇立即产生白雾,当用水浴加热后,无气泡产生,生成粘稠状液体,集气瓶C中有无色液体产生. |
请回答下列问题:
(1)写出装置中仪器A的名称;
(2)装置中B、C之间长导管的作用是 , 浓硫酸的作用是;
(3)实验二中,完成水浴加热必需的玻璃仪器有、;
(4)实验一、二中当加入无水乙醇时,均有白雾产生,请简述产生白雾的原因:;
(5)经检验集气瓶C中无色液体为磷酸三乙酯,请在图中虚线框内画出实验装置(含试剂)用于验证生成的乙烯;
(6)根据实验现象判断以P2O5作为催化剂获得乙烯的反应条件是 .
【题目】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空: 步骤一:配制250mL 0.1000mol/L NaOH标准溶液.
步骤二:取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作4次,记录数据如表.
实验编号 | NaOH溶液的浓度 | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 20.02 | 20.00 |
2 | 0.10 | 20.00 | 20.00 |
3 | 0.10 | 19.98 | 20.00 |
(1)步骤一需要称量氢氧化钠固体的质量为g,配制标准溶液需要用到玻璃棒,烧杯外,还需要的玻璃仪器有 .
(2)步骤二中量取20.00mL的稀盐酸用到的仪器是 . 判断滴定终点的现象是 .
(3)根据上述数据,可计算出该盐酸的浓度为 .
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏高的有
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,仰视读出滴定管读数;
E.碱式滴定管尖嘴部分有气泡,滴定后消失.
