题目内容
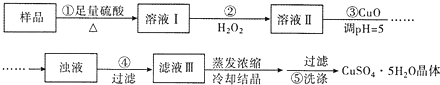
【题目】某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu (NO3)2的部分工艺流程如图所示:
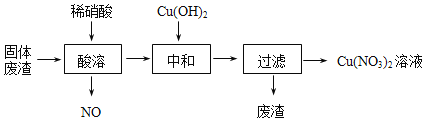
(1)Cu2O与稀硝酸反应的离子方程式为 。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是 ,若保持反应温度为70℃,欲加快反应速率可采取的措施为 (写出一种即可)。
(3)过滤后所得废渣的主要成分的化学式为 。
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为 ,由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法是:蒸发浓缩、 、过滤、冰水洗涤、 。
【答案】(1)3Cu2O +14H++ 2NO3-= 6Cu2++2NO↑+7H2O
(2)防止温度过高HNO3分解(或者挥发); 搅拌、将固体废渣粉碎、适当提高硝酸的浓度
(3)SiO2
(4)2 Cu(NO3)2 ![]() 2 CuO+4 NO2↑+ O2 冷却结晶 低温烘干
2 CuO+4 NO2↑+ O2 冷却结晶 低温烘干
【解析】
试题分析:(1)Cu2O中铜元素的化合价为+1价,具有还原性,能与硝酸发生氧化还原反应生成硝酸铜、NO和水,根据得失电子守恒、电荷守恒和原子守恒配平,反应的离子方程式为3Cu2O+14H ++2NO3-= 6Cu2++2NO↑+7H2O。
(2)为了防止温度过高HNO3分解,所以酸溶时,反应温度不宜超过70℃;根据影响化学反应速率的因素,若保持反应温度为70℃,欲加快反应速率可采取的措施为搅拌、将固体废渣粉碎、适当提高硝酸的浓度。
(3)Cu、CuO、Cu2O和SiO2这四种物质,只有SiO2和硝酸不反应,所以过滤后所得废渣的主要成分是二氧化硅,化学式为SiO2。
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,则该反应的化学方程式为2 Cu(NO3)2![]() 2 CuO+4NO2↑+ O2;根据硝酸铜的溶解性特征及受热易分解的性质,由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法是:蒸发浓缩、冷却结晶、过滤、冰水洗涤、低温烘干。
2 CuO+4NO2↑+ O2;根据硝酸铜的溶解性特征及受热易分解的性质,由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法是:蒸发浓缩、冷却结晶、过滤、冰水洗涤、低温烘干。

 53随堂测系列答案
53随堂测系列答案