题目内容
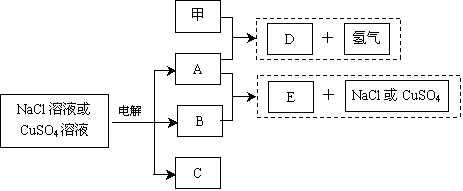
下图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法不正确的是( )
A.Y的氢化物比X的氢化物更稳定
B.原子半径大小顺序是Z>Y>X>R
C.Z的单质能与Y的某些化合物发生置换反应
D.X、Y、Z三种元素中,其最高价氧化物对应水化物的酸性强弱顺序是Z>Y>X
| | R | |
| X | Y | Z |
B.原子半径大小顺序是Z>Y>X>R
C.Z的单质能与Y的某些化合物发生置换反应
D.X、Y、Z三种元素中,其最高价氧化物对应水化物的酸性强弱顺序是Z>Y>X
B
X原子最外层电子数比次外层电子数少3,则X是P,所以Y是S,R是O,Z是Cl。同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐最大,所以选项B不正确,原子半径应该是X>Y>Z>R,其余都是正确的,答案选B。

练习册系列答案
相关题目

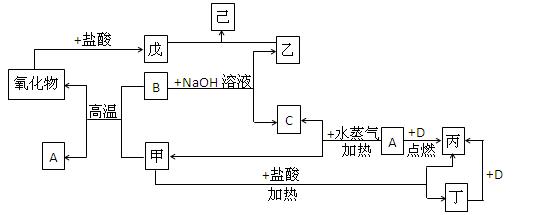
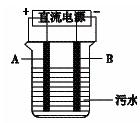
 液反应,其化学式为_▲_。
液反应,其化学式为_▲_。