题目内容
结合下表回答下列问题:
(1)CuCl2溶液中含有少量的FeCl2和FeCl3,为得到纯净的CuCl2?2H2O晶体,可先加入适量氯水,发生的离子反应为:_________________________________;再加入_______________________,调至pH=4,此时溶液中的c(Fe3+)=__________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2?2H2O晶体。
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,由CuCl2?2H2O晶体得到纯的无水CuCl2的合理方法是___________________________________________。
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,由CuCl2?2H2O晶体得到纯的无水CuCl2的合理方法是___________________________________________。
(1)2Fe2++ Cl2 = 2Fe3++ 2Cl-;CuO或Cu(OH) 2或CuCO3; 4×10-8mol/L
(2)在HCl气氛中蒸发结晶。
(2)在HCl气氛中蒸发结晶。
试题分析:(1)氯水的氧化性能把二价铁离子氧化成三价铁离子
(2)在HCl气氛中,隔绝了与空气的反应,不容易使杂质介入

练习册系列答案
相关题目




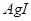 沉淀中滴入浓KCI溶液有白色沉淀出现
沉淀中滴入浓KCI溶液有白色沉淀出现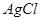 比
比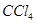 振荡,静置,下层溶液为紫色
振荡,静置,下层溶液为紫色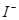

 分别在溶液中达到沉淀溶解平衡后,改变溶液
分别在溶液中达到沉淀溶解平衡后,改变溶液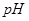 ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是

 固体可使溶液由
固体可使溶液由 点变到
点变到 点
点
 两点代表的溶液中
两点代表的溶液中 与
与 乘积相等
乘积相等 、
、 分别在
分别在 6Cu+SO2↑,该反应的氧化剂是_____;验证反应产生的气体是SO2的方法是____________。
6Cu+SO2↑,该反应的氧化剂是_____;验证反应产生的气体是SO2的方法是____________。
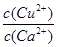 >
>
 Ca2+(aq)+2OH-(aq),当向一定量的石灰乳悬浊液中加入少量生石灰时,下列说法正确的是
Ca2+(aq)+2OH-(aq),当向一定量的石灰乳悬浊液中加入少量生石灰时,下列说法正确的是